แรงยึดเหนี่ยวภายในโมเลกุล
โดยปกติแล้วในธรรมชาติ อะตอมของธาตุต่าง ๆ จะไม่อยู่อย่างโดดเดี่ยว แต่จะรวมกันเป็นกลุ่มอะตอมหรือเป็นโมเลกุลของสารประกอบ เช่น HCl , NH3 เป็นต้น การที่อะตอมเหล่านี้รวมอยู่ด้วยกันได้อย่างเสถียรภาพนั้น เพราะมีแรงยึดเหนี่ยวอะตอมเหล่านั้น แรงยึดเหนี่ยวนี้เรียกว่า พันธะเคมี (chemical bond) ดังนั้นถ้าต้องการให้อะตอมที่รวมกันเป็นโมเลกุลแตกออกจากกัน ก็จะต้องมีการทำลายพันธะเคมีอันนี้ จึงสรุปคำจำกัดความของพันธะเคมี คือ แรงยึดเหนี่ยวอะตอมต่างๆ ให้อยู่ด้วยกันอย่างมีเสถียรภาพ เกิดเป็นโมเลกุลของสารประกอบ การที่อะตอมต่างๆ รวมกันอยู่ได้นั้นก็เพราะว่าสภาพรวมมีความเสถียรภาพมากกว่าที่จะอยู่ในสภาพโดดเดี่ยว อย่างไรก็ตามอะตอมของธาตุบางธาตุ เช่น ธาตุหมู่ 8 A (แก๊สเฉื่อย) ก็สามารถที่จะอยู่ได้ตามลำพัง โดยไม่ต้องรวมกับอะตอมอื่น เมื่อพิจารณาโครงสร้างและการจัดเรียงอิเล็กตรอนในอะตอมของแก๊สเฉื่อย จะพบว่าอะตอมเหล่านี้มีอิเล็กตรอนวงนอกสุด ครบจำนวน 8 ตัว ซึ่งเป็นการจัดอิเล็กตรอนที่เสถียรเป็นพิเศษ ดังนั้นอะตอมต่าง ๆ ที่เข้าทำปฏิกิริยากันก็จะพยายามเปลี่ยนแปลงและปรับจำนวนอิเล็กตรอนระดับวงนอกของตัวเองให้เป็นเหมือนแก๊สเฉื่อย ซึ่งมีจำนวนอิเล็กตรอนเท่ากับ 8 ซึ่งเป็นไปตามกฎที่เรียกว่า กฎออกเตต (octet rule) การปรับตัวของอะตอมเพื่อให้เป็นไปตามกฎออกเตตนั้น ทำได้โดยการให้อิเล็กตรอนไปกับอะตอมอื่น การรับอิเล็กตรอนจากอะตอมอื่น และการใช้อิเล็กตรอนร่วมกันกับอะตอมอื่น โมเลกุลของสารประกอบที่ปรับตัวเป็นไปตามกฎออกเตตนั้น โมเลกุลจะมีความเสถียรมาก
พัฒนาการของตารางธาตุ ตลอดจนแนวคิดของการจัดอิเล็กตรอน ช่วยให้นักเคมีสามารถอธิบายการเกิดโมเลกุลหรือสารประกอบได้อย่างมีเหตุผล กิลเบิร์ต ลิวอิส (Gilbert Newton Lewis) เสนอว่า อะตอมรวมตัวกันเพื่อทำให้เกิดการจัดอิเล็กตรอนที่มีเสถียรภาพเพิ่มขึ้น โดยเสถียรภาพมีค่ามากที่สุดเมื่ออะตอมมีจำนวนอิเล็กตรอนเท่ากับจำนวนอิเล็กตรอนในธาตุเฉื่อย เมื่ออะตอมรวมกันเกิดเป็นพันธะเคมี อิเล็กตรอนระดับนอกหรือที่เรียกว่า เวเลนซ์อิเล็กตรอนเท่านั้นที่เกี่ยวข้องกับการเกิดพันธะเคมี นักเคมีใช้สัญลักษณ์แบบจุดของลิวอิส ในการนับจำนวนเวเลนซ์อิเล็กตรอนระหว่างปฏิกิริยา และเพื่อให้แน่ใจว่าจำนวนอิเล็กตรอนมีค่าคงที่ สัญลักษณ์แบบจุดของลิวอิส ประกอบด้วยสัญลักษณ์ ธาตุ และจุด 1 จุด แทน 1 เวเลนซ์อิเล็กตรอนของอะตอมธาตุนั้น เช่น โลหะในหมู่ I Aซึ่งมีเวเลนซ์ อิเล็กตรอน 1 ตัว จะมีสัญลักษณ์ ดังนี้
ตารางที่ 2 แสดงสัญลักษณ์แบบจุดของลิวอิสของธาตุเรพรีเซนเททิฟในคาบที่ 2 และ 3
การจัดอิเล็กตรอนและตำแหน่งในตารางธาตุ สามารถนำมาทำนายชนิดพันธะที่เกิดขึ้นจำนวนพันธะที่เกิดขึ้น จำนวนพันธะที่อะตอมธาตุหนึ่ง ๆ จะสร้างได้รวมถึงเสถียรภาพของสารประกอบที่เกิดขึ้น
พันธะไอออนิก ( Ionic bond )
เป็นพันธะที่เกิดจากการที่อะตอมหนึ่งเป็นฝ่ายให้อิเล็กตรอนระดับนอก และอีกอะตอมหนึ่งเป็นฝ่ายรับอิเล็กตรอนเข้ามาสู่ระดับนอก แล้วทำให้อะตอมทั้งสองฝ่ายอยู่ในสภาพเสถียร (ครบ 8 ตามกฎออกเตต) เช่น ธาตุในหมู่ 1A ซึ่งมีเวเลนซ์อิเล็กตรอนเท่ากับ 1 ถ้าเอาอิเล็กตรอนตัวนี้ออกไปเสีย อิเล็กตรอนในระดับถัดเข้าไปจะมีจำนวนเท่ากับ 8 ซึ่งเป็นโครงสร้างที่เสถียรเหมือนแก๊สเฉื่อย เช่น Na มีโครงสร้างอิเล็กตรอนเป็น 1s2 2s22p6 3s1 ถ้าเอาอิเล็กตรอน 3s1 ออกไป จะเกิดเป็น Na+ จะมีโครงสร้างอิเล็กตรอนเป็น 1s2 2s2 2p6 ซึ่งมีเวเลนซ์อิเล็กตรอนเท่ากับ 8 ซึ่งเป็นโครงสร้างที่เสถียรเหมือนแก๊สเฉื่อย คือ Ne ซึ่งมีโครงสร้างอิเล็กตรอนคือ 1s2 2s2 2p6 ส่วนธาตุในหมู่ 7A มีเวเลนซ์อิเล็กตรอนเท่ากับ 7 ต้องการอีก 1 ตัว จะครบ 8 เช่น Cl มีโครงสร้างอิเล็กตรอนเป็น 1s2 2s2 2p6 3s2 3p5 ถ้ารับอิเล็กตรอนเข้ามาหนึ่งตัวจะกลายเป็น Cl – โครงสร้างอิเล็กตรอนจะเปลี่ยนเป็น 1s2 2s2 2p6 3s2 3p6 ซึ่งเหมือนโครงสร้างอิเล็กตรอนของ Ar ซึ่งเป็นธาตุเฉื่อย
อะตอมที่มีอิเล็กตรอนระดับนอกจำนวนน้อย มีพลังงานการแตกตัวเป็นไอออนต่ำและมีสัมพรรคภาพอิเล็กตรอนต่ำ มีแนวโน้มที่จะเสียอิเล็กตรอนระดับนอกไปแล้วกลายเป็นไอออนบวก ส่วนธาตุที่มีอิเล็กตรอนระดับนอกมากมีพลังงานการแตกตัวเป็นไอออนสูง มีสัมพรรคภาพอิเล็กตรอนสูง มีแนวโน้มจะรับอิเล็กตรอนได้ง่ายและกลายเป็นไอออนลบ เมื่ออะตอมเหล่านี้ถ่ายโอนอิเล็กตรอนให้แก่กันแล้วเกิดเป็นไอออนบวกและไอออนลบ ซึ่งมีประจุไฟฟ้าต่างกันจึงเกิดแรงดึงดูดกันทางไฟฟ้ายึดเหนี่ยวให้ไอออนทั้งสองอยู่ด้วยกัน พันธะระหว่างไอออนบวกและไอออนลบนี้เรียกว่า พันธะไอออนิก หรือพันธะอิเล็กโทรเวเลนซ์ และเรียกสารประกอบที่เกิดขึ้นว่า สารประกอบไอออนิก
พันธะไอออนิกเกิดได้ง่ายระหว่างธาตุที่กลายเป็นไอออนบวกได้ง่าย เช่น ธาตุหมู่ 1A และหมู่ 2 A กับธาตุที่กลายเป็นไอออนลบได้ง่าย เช่น ธาตุหมู่ 7A และ 6 A ตัวอย่างเช่น
มีหลายกรณีที่ไอออนบวกกับไอออนลบในสารประกอบมีประจุต่างกัน เช่น เผาลิเทียม (Li) ในอากาศได้เป็นลิเทียมออกไซด์ (Li2O) ดังสมการ
สัญลักษณ์ลิวอิสแสดงการเกิด LiO2 สามารถเขียนได้ดังนี้
พันธะไอออนิกไม่มีทิศทางที่แน่นอน เพราะเกิดจากแรงดึงดูดทางไฟฟ้าระหว่างไอออนบวกกับไอออนลบ
สารประกอบไอออนิก
สารประกอบไอออนิก เป็นสารประกอบที่ประกอบด้วยไอออนที่มาอยู่รวมกันยึดเหนี่ยวกันด้วยพันธะไอออนิกคือแรงดึงดูดทางไฟฟ้าระหว่างไอออนที่มีประจุตรงข้ามกัน การที่ไอออนรวมกันอยู่เป็นกลุ่มทำให้สารประกอบไอออนิกมีสมบัติ ดังนี้
1.การละลาย สารประกอบไอออนิก ส่วนมากละลายน้ำได้ ไม่ละลายในตัวทำละลายที่เป็นสารอินทรีย์อื่น ๆ จากความสามารถละลายน้ำได้ จะพบสารประกอบไอออนิกละลายอยู่ในน้ำทะเลและมหาสมุทร เช่น NaCl เป็นต้น
2.การนำไฟฟ้า สารประกอบไอออนิกในสภาพของแข็ง มีการนำไฟฟ้าต่ำมาก เพราะไอออนเกาะกันแน่นในโครงสร้างของผลึก จึงไม่สามารถเคลื่อนที่อย่างอิสระได้ แต่เมื่อละลายน้ำเป็นสารละลาย หรืออยู่ในสภาวะหลอมเหลวจะนำไฟฟ้าได้ดี ทั้งนี้เนื่องจากเกิดการแตกตัวเป็นไอออน และไอออนเหล่านี้เคลื่อนที่ได้เป็นอิสระภายใต้สนามไฟฟ้า เช่น การทำอิเล็กโทรไลซิสเกลือชนิดต่าง ๆ
3.ความแข็ง สารประกอบไอออนิกโดยทั่วไปเป็นของแข็ง ภายในผลึกประกอบด้วยแรงยึดเหนี่ยวระหว่างไอออนที่เกิดจากไฟฟ้าสถิตที่แข็งแรงมากจากการทดลองโดยใช้รังสีเอ็กซ์ ศึกษาโครงสร้างผลึกโซเดียมคลอไรด์ พบว่ามีกลุ่มอิเล็กตรอน 2 กลุ่ม กลุ่มหนึ่งมีอิเล็กตรอน 10 ตัว อีกกลุ่มหนึ่งมีอิเล็กตรอน 18 ตัว ล้อมรอบนิวเคลียสหนึ่ง ๆ จำนวนอิเล็กตรอน 2 กลุ่มนี้ตรงกับจำนวนอิเล็กตรอนของโซเดียมไอออนและคลอไรด์ไอออน ตามลำดับ สมบัติที่เกี่ยวกับความแข็งของสารประกอบไอออนิกเนื่องมาจาก การดึงดูดกันระหว่างไอออนในโครงสร้างของผลึก
4.จุดเดือดและจุดหลอมเหลว สารประกอบไอออนิกมีแนวโน้มที่จะมีจุดเดือดและจุดหลอมเหลวสูง เนื่องจากมีพันธะไอออนิกที่แข็งแรง และมีแรงดึงดูดระหว่างไอออนบวกและไอออนลบทุกทิศทาง เช่น NaCl เมื่อพิจารณาในโครงสร้างของผลึก พบว่า แต่ละ Na+ จะดึงดูดกับ Cl– ไอออน ที่อยู่ล้อมรอบ และขณะเดียวกันแต่ละ Cl– จะดึงดูดกับ Na+ 6 ไอออนการดึงดูดจะเป็นไปในลักษณะเช่นนี้ตลอดทั้งผลึก และเป็นผลให้ NaCl มีจุดหลอมเหลวสูง
(ที่มา : http://projects.edte.utwente.nl/deeltjesmodel/FS-register.html)
ปฏิกิริยาของโซเดียมกับคลอรีน เกิดขึ้นเพียงขั้นเดียวมากกว่าที่จะมีหลายขั้นตอนแต่การคำนวณการเปลี่ยนแปลงพลังงาน อาจทำให้สะดวกขึ้นถ้าแบ่งปฏิกิริยาเป็น 5 ขั้นตอน ดังนี้
1. การเปลี่ยนสถานะของโลหะโซเดียมจากของแข็งไปเป็นไอ (การระเหิด)
2. การสลายตัวของคลอรีนโมเลกุลเป็นคลอรีนอะตอม ใช้พลังงาน 243 kJ/mol ของ Cl2
3. การเปลี่ยนโซเดียมอะตอมให้เป็นโซเดียมไอออน (ค่า IE)
4. การเปลี่ยนคลอรีนอะตอมให้เป็นคลอไรด์ไอออน (ค่า EA)
5. การรวมกันของโซเดียมไอออนและคลอไรด์ไอออนเป็น NaCl การเปลี่ยนแปลงพลังงานในขั้นตอนนี้ ขึ้นกับแรงดึงดูดระหว่างประจุ ซึ่งเป็นพลังงานที่ปลดปล่อย มีค่าเท่ากับ -787 kJ/Mol สำหรับ NaCl
รวมปฏิกิริยา 5 ขั้นตอนและการเปลี่ยนแปลงพลังงานได้ ดังนี้
ผลรวมของการเปลี่ยนแปลงพลังงานทั้ง 5 ขั้นตอนเท่ากับการเปลี่ยนแปลงพลังงานสุทธิของปฏิกิริยารวม ซึ่งแสดงเป็นแผนภาพขั้นตอนการเปลี่ยนแปลงพลังงานในปฏิกิริยาระหว่างโซเดียมและคลอรีน เรียกว่า วัฏจักรบอร์น-ฮาเบอร์ (Born-Haber cycle) ดังนี้
ภาพวัฏจักรบอร์น – ฮาเบอร์
จากแผนภาพจะเห็นว่าขั้นตอนที่ 1, 2 และ 3 เป็นขั้นตอนการดูดพลังงาน (การเปลี่ยนแปลงพลังงานมีค่าเป็น +) ในขณะที่ขั้นตอนที่ 4 และ 5 เป็นขั้นตอนการคายพลังงาน โดยเฉพาะขั้นตอนที่ 5 นั้นเป็นการสร้างพันธะไอออนิก
พันธะโคเวเลนต์ (Covalent bond)
พันธะโคเวเลนต์ เป็นพันธะที่เกิดขึ้นเมื่ออะตอมสร้างแรงยึดเหนี่ยวระหว่างกัน นำเอาอิเล็กตรอนระดับนอกที่มีจำนวนเท่ากันมาใช้ร่วมกัน (Share) อาจจะเป็น 1 คู่ เกิดพันธะเดี่ยว (Single bond) 2 คู่ เกิดพันธะคู่ (Double bond) หรือ 3 คู่ เกิดพันธะสาม (triple bond) สารประกอบที่เกิดขึ้นจากการเกิดพันธะโคเวเลนต์ เรียกว่า สารประกอบโคเวเลนต์ ในปี ค.ศ. 1916 กิลเบิร์ต ลิวอิส (Gilbert Lewis) ได้เสนอแนวคิดว่า พันธะโคเวเลนต์เป็นเรื่องของการใช้อิเล็กตรอนร่วมกันระหว่าง 2 อะตอมที่เข้าทำปฏิกิริยากัน ขณะเดียวกันก็มีการเปลี่ยนแปลงจำนวนอิเล็กตรอนรอบนอกสุด ให้มีการจัดเรียงอิเล็กตรอนครบ 8 ตัว แบบแก๊สเฉื่อย ซึ่งเป็นไปตามกฎออกเตต ตัวอย่าง เช่น ฟลูออรีน มีอิเล็กตรอน ระดับนอก 7 ตัว ต้องการอีก 1 ตัว จะครบ 8 เหมือน Ne เมื่อ ฟลูออรีนอะตอม (F2) มารวมกันจะสร้างพันธะโคเวเลนต์ชนิดพันธะเดี่ยวจะได้โมเลกุล F2 มีโครงสร้างลิวอิสดังนี้
เพื่อความสะดวกและชัดเจนจะใช้ขีด (-) สั้น ๆ แทนอิเล็กตรอนหนึ่งคู่ที่ใช้ร่วมกัน จะสังเกต เห็นว่ามีอิเล็กตรอนระดับนอกที่ไม่ได้เกี่ยวข้องกับการเกิดพันธะ เรียกว่า อิเล็กตรอนไม่ร่วมพันธะ (nonbonding electron) หรือ อิเล็กตรอนคู่โดดเดี่ยว (lone pair electron) ซึ่งใน F2 จะมีอิเล็กตรอนคู่โดดเดี่ยวอยู่อะตอมละ 3 คู่
ในทำนองเดียวกันออกซิเจนมีอิเล็กตรอนระดับนอก 6 ตัว ต้องการอีก 2 ตัว จะครบ 8 เมื่อออกซิเจน 2 อะตอม มารวมกันจะเกิดเป็นโมเลกุลออกซิเจน (O2) มีโครงสร้างลิวอิส ดังนี้
ไนโตรเจนก็เช่นกันจะใช้อิเล็กตรอนร่วมกัน 3 คู่ เกิดเป็นโมเลกุลไนโตรเจน ( N2 ) และมีอิเล็กตรอนคู่โดดเดี่ยวอะตอมละ 1 คู่ เขียนโครงสร้างลิวอิสได้ดังนี้
กฎออกเตต (Octet rule)
ลิวอิส ได้เสนอกฎออกเตต ซึ่งกฎนี้กล่าวว่า อะตอมต่าง ๆ นอกจากไฮโดรเจนมีแนวโน้มจะสร้างพันธะ เพื่อให้มีอิเล็กตรอนระดับนอกครบแปด อะตอมจะสร้างพันธะโคเวเลนต์ เมื่อมีอิเล็กตรอนระดับนอกไม่ครบ 8 อิเล็กตรอน (เรียกว่า ไม่ครบออกเตต) การใช้อิเล็กตรอนร่วมกันในพันธะโคเวเลนต์ จะทำให้อะตอมมีอิเล็กตรอนครบออกเตตได้ ยกเว้นไฮโดรเจนจะสร้างพันธะเพื่อให้มีการจัดอิเล็กตรอนระดับนอกเหมือนธาตุฮีเลียม คือ มี 2 อิเล็กตรอน เช่น
ข้อยกเว้นของกฎออกเตต
กรณีโมเลกุลที่อะตอมกลางมีอิเล็กตรอนเกินแปด ธาตุบางธาตุในคาบที่ 3 เช่น ฟอสฟอรัส (P) หรือ กำมะถัน (S) สามารถมีอิเล็กตรอนระดับนอกได้เกิน 8 ตัว (เพราะจำนวนอิเล็กตรอนในระดับพลังงาน n = 3 มีอิเล็กตรอนได้สูดสุด 18 ตัว) จึงทำให้ฟอสฟอรัสและกำมะถัน สามารถสร้างพันธะโคเวเลนต์ โดยใช้อิเล็กตรอนมากกว่า 8 ตัว ได้ เช่น ฟอสฟอรัสเพนตะคลอไรด์ (PCl5)
กรณีของโมเลกุลที่อะตอมกลางมีอิเล็กตรอนไม่ครบแปดในสารประกอบบางชนิด อะตอมกลางของโมเลกุลที่เสถียรมีอิเล็กตรอนไม่ครบ 8 อิเล็กตรอน เช่น โบรอนไตรฟลูออไรด์ (BF3 )
จะเห็นว่าโบรอน (B) มีอิเล็กตรอนเพียง 6 อิเล็กตรอน ซึ่งไม่ครบออกเตต นอกจากนี้โมเลกุลที่อะตอมกลางมีอิเล็กตรอนเป็นจำนวนเลขคี่ โมเลกุลบางชนิดมีอิเล็กตรอนล้อมรอบเป็นจำนวนเลขคี่ และไม่ครบออกเตตทุกอะตอม เช่น ไนโตรเจนไดออกไซด์ (NO2)
ไนโตรเจน (N) มีอิเล็กตรอนล้อมรอบไม่ครบ 8 มีเพียง 7 อิเล็กตรอน ในบางกรณี อิเล็กตรอนคู่ที่ใช้ร่วมกันในการสร้างพันธะโคเวเลนต์ไม่ได้มาจากอะตอมสองอะตอม อาจมาจากอะตอมเดียว เช่น โมเลกุลแอมโมเนียรวมกับไฮโดรเจนไอออนได้เป็น แอมโมเนียมไอออน (NH3+H+ NH4+) ซึ่งแอมโมเนียมีอิเล็กตรอนคู่โดดเดี่ยว 1 คู่ สามารถใช้ร่วมกับไฮโดรเจนไอออนได้ ดังนี้
พันธะโคเวเลนต์ที่เกิดขึ้นใหม่ระหว่าง NH3 กับ H+ เรียกว่า พันธะโคออร์ดิเนตโคเวเลนต์ หรือพันธะเดทีฟ ซึ่งมีสมบัติเหมือนพันธะโคเวเลนต์ธรรมดา เพราะพันธะทั้ง 4 ของ NH4+ มีสมบัติเหมือนกันทุกประการ
ความยาวพันธะและพลังงานพันธะ
ความยาวพันธะ หมายถึง ระยะระหว่างนิวเคลียสของอะตอมที่สร้างพันธะกันซึ่งเป็นค่าที่วัดได้ในหน่วย พิกโคเมตร (pm) และพลังงานพันธะ หมายถึง พลังงานที่ใช้ในการแยกอะตอม ที่ยึดเหนี่ยวกันไว้ด้วยพันธะให้หลุดออกจากกัน วัดได้ในหน่วยกิโลจูลต่อโมล พลังงานพันธะบอกให้ทราบถึงความแข็งแรงของพันธะนั้น พันธะยิ่งแข็งแรงยิ่งต้องการพลังงานมากในการทำลายพันธะ พลังงานพันธะบางครั้งเรียก พลังงานสลายพันธะ ความยาวพันธะและพลังงานพันธะขึ้นอยู่กับปริมาณความหนาแน่นของอิเล็กตรอนระหว่างนิวเคลียสของอะตอมทั้งสอง ถ้าความหนาแน่นอิเล็กตรอนมาก นิวเคลียสทั้งสองจะยึดเหนี่ยวกันไว้อย่างแรง และเข้ามาอยู่ชิดกันมาก ดังนั้นพันธะคู่จะสั้นและแข็งแรงกว่าพันธะเดี่ยวและพันธะสามจะสั้นและแข็งแรงกว่าพันธะคู่
เรโซแนนซ์
เรโซแนนซ์ หมายถึง การใช้โครงสร้างลิวอิสตั้งแต่ 2 โครงสร้างขึ้นไปแทนโมเลกุลใดโมเลกุลหนึ่งที่ไม่สามารถเขียนโครงสร้างที่แท้จริงออกมาเป็นสูตรได้อย่างชัดเจน เช่น เบนซีน จากการทดลองพบว่าพันธะระหว่างคาร์บอนอะตอมในโครงสร้างทั้ง 6 พันธะยาวเท่ากันคือ 140 pm ซึ่งอยู่ระหว่างความยาวของพันธะเดี่ยว c – c เท่ากับ 154 pm และความยาวของพันธะคู่ c = c เท่ากับ 133 pm แสดงว่าโครงสร้างเรโซแนนซ์ที่เขียนขึ้นนี้ไม่ใช่โครงสร้างที่แท้จริงของเบนซีน โครงสร้างที่แท้จริงของเบนซีนเป็นเรโซแนนซ์ไฮบริดของโครงสร้าง
เรโซแนนซ์ทั้งสองที่เขียนดังตัวอย่างต่อไปนี้
รูปร่างของโมเลกุลโคเวเลนต์และทฤษฎี VSERP
รูปร่างของโมเลกุลโคเวเลนต์ เป็นสมบัติที่สำคัญของโมเลกุล เนื่องจากรูปร่างของโมเลกุลจะมีผลต่อสมบัติทางกายภาพ และปฏิกิริยาเคมี เราสามารถทราบสูตรของสารประกอบโคเวเลนต์ได้จากการเขียนโครงสร้างลิวอิส พิจารณาโมเลกุลของน้ำ (H2O) ซึ่งในที่นี้แสดงการเขียนโครงสร้างลิวอิสได้ 6 แบบ ดังนี้
จะเห็นว่าโครงสร้างลิวอิส ไม่สามารถใช้แสดงรูปร่างของโมเลกุลได้ แต่ใช้อธิบายการเกิดพันธะระหว่างอะตอมใน 2 มิติ เช่น โครงสร้างลิวอิสของน้ำ บอกให้ทราบว่า ไฮโดรเจน 2 อะตอม เกิดพันธะโคเวเลนต์ชนิดพันธะเดี่ยวกับออกซิเจน ซึ่งเป็นอะตอมกลางและมีอิเล็กตรอนคู่โดดเดี่ยว 2 คู่ ถ้าเขียนโครงสร้างลิวอิสของโมเลกุลมีเทน (CH4) พบว่าคู่อิเล็กตรอนทั้ง 4 คู่รอบคาร์บอน ซึ่งเป็นอะตอมกลาง เป็นอิเล็กตรอนคู่สร้างพันธะ จึงเขียนให้ทุกอะตอมอยู่ในแนวระนาบเดียวกัน ไม่ได้แสดงรูปร่างที่แท้จริงของโมเลกุล จากการศึกษาพบว่าโมเลกุลของมีเทนมีรูปร่างเป็นทรงสี่หน้า (tetrahedral) ดังภาพ
ภาพที่ 24 โมเลกุลของมีเทน
รูปร่างของโมเลกุลขึ้นกับมุมพันธะ (bond angle) ส่วนขนาดของโมเลกุลขึ้นกับความยาวพันธะ (bond langht) ซึ่งเป็นระยะทางระหว่างนิวเคลียสของอะตอมที่เกิดพันธะกัน ทฤษฎีที่ใช้ทำนายรูปร่างของโมเลกุลโคเวเลนต์คือ ทฤษฎีการผลักกันของคู่อิเล็กตรอนวงนอกสุด (Valence Shell Electron Pair Repulsion) เรียกสั้นๆว่าทฤษฎี VSEPR ทฤษฎีนี้มีสมมุติฐานเกี่ยวกับการเกิดพันธะดังนี้
1.อะตอมต่าง ๆ ในโมเลกุล เกิดพันธะกันด้วยคู่อิเล็กตรอนวงนอกสุดโดยอะตอมเกิดพันธะกันด้วยอิเล็กตรอนคู่สร้างพันธะ 1 คู่ (พันธะเดี่ยว) หรือมากกว่า
2.อะตอมบางอะตอมในโมเลกุล อาจมีอิเล็กตรอนคู่ที่ไม่สร้างพันธะหรืออิเล็กตรอนคู่โดดเดี่ยว (lone pair)
3.อิเล็กตรอนคู่สร้างพันธะ และอิเล็กตรอนคู่โดดเดี่ยว รอบอะตอมใด ๆในโมเลกุลเป็นกลุ่ม หมอกอิเล็กตรอนที่มีประจุลบ จึงพยายามอยู่ห่างกันให้มากที่สุดเพื่อให้มีแรงผลักซึ่งกันและกันของคู่อิเล็กตรอนน้อยที่สุดและพลังงานของโมเลกุลมีค่าน้อยที่สุด
4.อิเล็กตรอนคู่โดดเดี่ยวครอบครองที่ว่างมากกว่าอิเล็กตรอนคู่สร้างพันธะ โดยที่แรงผลักของอิเล็กตรอนสามารถเรียงลำดับได้ดังนี้ อิเล็กตรอนคู่โดดเดี่ยว – อิเล็กตรอนคู่โดดเดี่ยว > อิเล็กตรอนคู่โดดเดี่ยว – อิเล็กตรอนคู่สร้างพันธะ > อิเล็กตรอนคู่สร้างพันธะ – อิเล็กตรอนคู่สร้างพันธะ
5.แรงผลักลดลงเมื่อมุมระหว่างอิเล็กตรอนกว้างขึ้น เช่น แรงผลักของคู่อิเล็กตรอนที่ทำมุม 90 องศาจะมากกว่าแรงผลักระหว่างคู่อิเล็กตรอนที่ทำมุม 120 องศา โมเลกุลที่อะตอมกลางมีคู่อิเล็กตรอน 2 คู่ คู่อิเล็กตรอนทั้งสองจะมีแรงผลักกันน้อยที่สุด เมื่ออยู่ตรงกันข้ามมุมระหว่างคู่อิเล็กตรอนทั้งสองเป็น 180๐ รูปทรงเรขาคณิตของคู่อิเล็กตรอนจึงเป็นเส้นตรง ดังรูป
โมเลกุลที่อะตอมกลางมีคู่อิเล็กตรอน 3 คู่ ดังรูป
โมเลกุลที่อะตอมกลางมีคู่อิเล็กตรอน 5 คู่ ดังรูป
a = อะตอมคู่สร้างพันธะ
ในแนว axial
e = อะตอมคู่สร้างพันธะ
ในแนว equatorial
วิธีทำนายรูปร่างของโมเลกุลโดยใช้ทฤษฎี VSEPR
การทำนายรูปร่างของโมเลกุลทำได้ดังต่อไปนี้
1.เขียนโครงสร้างลิวอิสของโมเลกุลหรือไอออน โดยให้อะตอมที่สนใจเป็นอะตอมกลางและอะตอมอื่น เกิดพันธะกับอะตอมที่สนใจโดยอาจเป็นพันธะเดี่ยว พันธะคู่หรือพันธะสาม
2.นับจำนวนคู่อิเล็กตรอนรอบอะตอมกลาง ทั้งอิเล็กตรอนคู่สร้างพันธะ และอิเล็กตรอนคู่โดดเดี่ยว
2.1 อิเล็กตรอนในพันธะคู่หรือพันธะสาม นับเป็นกลุ่มหมอกอิเล็กตรอน 1 กลุ่ม
2.2 อิเล็กตรอนคู่โดดเดี่ยว นับเป็นกลุ่มหมอกอิเล็กตรอน 1 กลุ่ม
2.3 สำหรับโมเลกุลหรือไอออนที่มีโครงสร้างเรโซแนนซ์ อาจใช้โครงสร้างเรโซแนนซ์ไฮบริดในการทำนายรูปร่างของโมเลกุล
3.ระบุรูปทรงเรขาคณิตของคู่อิเล็กตรอนที่เสถียรที่สุดได้แก่ เส้นตรง สามเหลี่ยมแบนราบ ทรงสี่หน้า พีระมิดคู่ฐานสามเหลี่ยมและทรงแปดหน้า
4.พิจารณาตำแหน่งของอะตอมตามชนิดของคู่อิเล็กตรอนในโมเลกุล สำหรับการจัดเรียงตัวของคู่อิเล็กตรอนแบบพีระมิดคู่ฐานสามเหลี่ยมและทรงแปดหน้านั้นอาจมีการจัดเรียงตัวของอิเล็กตรอนคู่สร้างพันธะและอิเล็กตรอนคู่โดดเดี่ยวได้มากกว่า 1 แบบ
4.1 พีระมิดคู่ฐานสามเหลี่ยม ให้อิเล็กตรอนคู่โดดเดี่ยวอยู่ในระนาบของฐานสามเหลี่ยม
4.2 ทรงแปดหน้า ถ้ามีอิเล็กตรอนคู่โดดเดี่ยว 2 คู่ ให้อิเล็กตรอนคู่โดดเดี่ยวแต่ละคู่อยู่คนละด้านของอะตอมกลาง
5.ระบุรูปร่างของโมเลกุลตามตำแหน่งของอะตอมไม่ใช้ตามคู่อิเล็กตรอนที่ล้อมรอบอะตอมกลาง
สภาพขั้วของโมเลกุล (Polarity of molecule)
โมเลกุลมีขั้ว (Polar molecule) คือโมเลกุลที่เป็นกลางซึ่งมีการกระจายของอิเล็กตรอนไม่สม่ำเสมอ ทำให้โมเลกุลมีขั้วบวกและขั้วลบ ซึ่งเรียกว่า เป็นขั้วคู่ (dipole) เนื่องจากมีขั้วบวก (ประจุบวกบางส่วน , ) และขั้วลบ (ประจุลบบางส่วน, ) โมเลกุลมีขั้วจะมีการจัดเรียงตัวในสนามไฟฟ้าโดยหันขั้วบวกของโมเลกุลเข้าหาขั้วไฟฟ้าลบ แต่เนื่องจากประจุสุทธิเป็นศูนย์ โมเลกุลมีขั้วจึงไม่เคลื่อนที่ในสนามไฟฟ้า ในขณะที่ไอออนต่าง ๆ เช่น Na+ และ Cl– จะเคลื่อนที่ในสนามไฟฟ้าได้ ส่วนโมเลกุลไม่มีขั้ว (nonpolar molecule) จะไม่มีการจัดเรียงตัวในสนามไฟฟ้า และไม่เคลื่อนที่ในสนามไฟฟ้า
ทฤษฎีพันธะเวเลนซ์ (Valence bond theory)
โครงสร้างลิวอิส และทฤษฎี VSEPR ให้ข้อมูลเกี่ยวกับรูปร่างของโมเลกุลและการกระจายของอิเล็กตรอนในโมเลกุล อย่างไรก็ตามทฤษฎี VSEPR ไม่ได้อธิบายว่าเหตุใดจึงเกิดพันธะ ในปี ค.ศ. 1930 ไลนัส พอลิง (Linus Pauling) และเจ.ซี. สเลเตอร์ (J.C. Slater) ได้เสนอทฤษฎีที่ใช้อธิบายการเกิดพันธะโคเวเลนต์ขึ้นเรียกว่า ทฤษฎีพันธะเวเลนซ์ (valence bond theory) โดยพันธะโคเวเลนต์เกิดขึ้นโดยออร์บิทัลอะตอมวงนอกสุดที่มีอิเล็กตรอนบรรจุอยู่เพียงตัวเดียวซ้อนเกย (Overlap) กับออร์บิทัลอะตอมวงนอกสุดที่มีอิเล็กตรอนตัวเดียวของอีกอะตอมหนึ่ง และอิเล็กตรอนทั้งสองจะจัดตัวให้มีสปินตรงกันข้ามอยู่ในออร์บิทัลนี้ เช่น ใน H2 พันธะ H-H เกิดจากการซ้อนเกยกันของ 1S ออร์บิทัล ดังรูป
ภาพที่ 25 พันธะ H – H เกิดจากการซ้อนเกยกันของ 1s ออร์บิทัลจากแต่ละไฮโดรเจนอะตอม
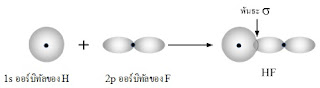
ในไฮโดรเจนฟลูออไรด์โมเลกุล HF พันธะเกิดจากการซ้อนกันของ 2p ออร์บิทัลของฟลูออรีนอะตอมกับ 1s ออร์บิทัลของไฮโดรจนอะตอม ดังรูป
ภาพที่ 26 พันธะ H – F เกิดจากการซ้อนกันของ 1s ออร์บิทัลของไฮโดรเจนอะตอมกับ 2p ออร์บิทัลของฟลูออรีนอะตอม
พันธะที่เกิดขึ้นจากการซ้อนกันของ s ออร์บิทัลกับ s ออร์บิทัลหรือ s ออร์บิทัลกับ p ออร์บิทัล เรียกว่า พันธะซิกมา (σ bond) ซึ่งเป็นพันธะโคเวเลนต์ที่มีความหนาแน่นของอิเล็กตรอนสูงในแนวแกนระหว่างนิวเคลียส อิเล็กตรอนเหล่านี้จะทำหน้าที่เป็น “กาว” ยึดนิวเคลียสทั้งสองไว้ด้วยกัน
P ออร์บิทัล 2 ออร์บิทัลอาจซ้อนกันได้ 2 แบบเนื่องจาก p ออร์บิทัลไม่เป็นทรงกลม ถ้า p ออร์บิทัลทั้งสองซ้อนกันตามแนวแกนระหว่างนิวเคลียส จะเกิดพันธะ σ แต่ถ้า p ออร์บิทัลทั้งสองซ้อนกันทางด้านข้างจะเกิดพันธะที่เรียกว่า พันธะพาย (π bond) พันธะ π นี้เป็นพันธะโคเวเลนต์ซึ่งบริเวณที่ซ้อนกันอยู่เหนือและใต้แกนระหว่างนิวเคลียส การซ้อนกันของ P ออร์บิทัลในพันธะ π เกิดขึ้นได้น้อยกว่าการซ้อนกันในพันธะ σ ดังนั้นพันธะπ จะแข็งแรงน้อยกว่าพันธะ σ
ภาพที่ 27 การเกิดพันธะโดยการซ้อนกันของ p ออร์บิทัล 2 ออร์บิทัล (ก) พันธะ σ และ (ข) พันธะ π
พันธะเดี่ยวจะเป็นพันธะ σ เสมอ พันธะคู่ประกอบด้วยพันธะ σ หนึ่งพันธะและพันธะ π หนึ่งพันธะ ส่วนพันธะสามประกอบด้วยพันธะ σ หนึ่งพันธะ และพันธะ π สองพันธะ
ออกซิเจนมีโครงสร้างอิเล็กตรอนเป็น 1s² 2s² 2p4
เนื่องจากออกซิเจนมีอิเล็กตรอนเดี่ยว 2 ตัวใน p ออร์บิทัล จึงสามารถเกิดพันธะกับออกซิเจนอีกอะตอมหนึ่งได้ 2 พันธะ พันธะหนึ่งเกิดจากการซ้อนกันของ p ออร์บิทัลในแนวแกนระหว่างนิวเคลียส เกิดเป็นพันธะ หนึ่งพันธะ อีกหนึ่งพันธะเกิดจากการซ้อนกันของ p ออร์บิทัลทางด้านข้าง เกิดเป็นพันธะ หนึ่งพันธะ พันธะใน O2 จึงเป็นพันธะคู่
ทฤษฎีไฮบริดออร์บิทัล (Hybrid obital theory)
ทฤษฎีพันธะเวเลนซ์สามารถอธิบายการเกิดพันธะในโมเลกุลอะตอมคู่และโมเลกุลง่าย ๆ ได้ดี อย่างไรก็ตามทฤษฎีดังกล่าวไม่สามารถอธิบายการเกิดพันธะในโมเลกุลอื่นอีกมากมายได้ เช่น มีเทน (CH4) คาร์บอนอะตอมมีอิเล็กตรอนวงนอกสุด 4 ตัว
จึงมี p ออร์บิทัลที่บรรจุอิเล็กตรอนเดียว 2 ออร์บิทัลซึ่งสามารถซ้อนกับ s ออร์บิทัลของไฮโดรเจนเกิดพันธะได้ แต่จากการทดลองพบว่าโมเลกุล CH4 มีรูปร่างเป็นทรงสี่หน้า มุมพันธะเป็น 109.50 โดยมีพันธะ ระหว่างคาร์บอนและไฮโดรเจน 4 อะตอม จำนวน 4 พันธะ ซึ่งทุกพันธะเหมือนกัน การที่จะเกิดพันธะ ตามแนวแกนพันธะได้ คาร์บอนอะตอมจะต้องมีออร์บิทัลที่ชี้ไปยังมุมของทรงสี่หน้า และซ้อนกับ 1s ออร์บิทัลของแต่ละไฮโดรเจนอะตอม อย่างไรก็ตาม นักศึกษาได้ทราบแล้วว่า s และ p ออร์บิทัลไม่ได้มีรูปร่างและการจัดเรียงตัวเป็นมุมดังกล่าว จึงเป็นไปไม่ได้ที่จะให้ 2s และ 2p ออร์บิทัลของคาร์บอนซ้อนกับ 1s ออร์บิทัลของไฮโดรเจนทั้งสี่อะตอม เกิดเป็นพันธะ สี่พันธะที่เหมือนกันและมีรูปร่างเป็นทรงสี่หน้า
ทฤษฎีไฮบริดออร์บิทัล กล่าวว่า “เมื่ออะตอม 2 อะตอมเข้าใกล้กัน อิทธิพลของนิวเคลียสของอะตอมทั้งสองจะทำให้พฤติกรรมของอิเล็กตรอนในแต่ละอะตอมเปลี่ยนแปลงไป ดังนั้นออร์บิทัลอะตอมที่เกิดพันธะจะแตกต่างไปจากออร์บิทัลอะตอมในอะตอมเดี่ยว เวเลนซ์ออร์บิทัลที่พลังงานใกล้เคียงกันของอะตอมเดียวกันจะเข้ามารวมกันเกิดเป็นออร์บิทัลอะตอมใหม่ ซึ่งมีรูปร่าง ทิศทาง และพลังงานเปลี่ยนไปจากเดิม” ออร์บิทัลอะตอมที่เกิดขึ้นใหม่นี้ เรียกว่าไฮบริดออร์บิทัลอะตอม (hybrid atomic orbitals) ซึ่งมักเรียกกันสั้น ๆว่า ไฮบริดออร์บิทัล (hybrid orbitals) จำนวนไฮบริดออร์บิทัลที่ได้นี้จะเท่ากับจำนวนออร์บิทัลอะตอมที่มารวมกัน ไฮบริดออร์บิทัลสามารถซ้อนกับออร์บิทัลของอะตอมอื่นได้ดีกว่า และเกิดพันธะที่แข็งแรงกว่าออร์บิทัลอะตอมเดิม กระบวนการที่ออร์บิทัลอะตอมรวมกันเกิดเป็นไฮบริดออร์บิทัล เรียกว่า ไฮบริไดเซชัน (hybridization)
ถ้าใช้ทฤษฎีไฮบริดออร์บิทัล เราจะอธิบายการเกิดพันธะในมีเทนได้ว่า เมื่อไฮโดรเจน 4 อะตอมเข้าใกล้คาร์บอนอะตอม เวเลนซ์ออร์บิทัลของคาร์บอนคือ 2s ออร์บิทัล 1 ออร์บิทัล และ 2p ออร์บิทัล 3 ออร์บิทัล จะรวมกันเป็น sp3 ไฮบริดออร์บิทัล 4 ออร์บิทัลซึ่งมีพลังงานเท่ากันและมีรูปร่างเหมือนกัน โดยแต่ละไฮบริดออร์บิทัลจะมี 2 พู พูหนึ่งมีขนาดใหญ่ อีกพูหนึ่งมีขนาดเล็ก พูใหญ่จะมีความยาวจากนิวเคลียสมากกว่า s และ p ออร์บิทัลที่ทำให้เกิดไฮบริดออร์บิทัลนั้น ทำให้ไฮบริดออร์บิทัลซ้อนกับออร์บิทัลของอะตอมอื่นได้ดีกว่าและเกิดพันธะที่แข็งแรงกว่าออร์บิทัลอะตอมเดิม sp3 ไฮบริดออร์บิทัลทั้งสี่จะจัดเรียงตัวให้อยู่ห่างกันมากที่สุดเพื่อลดแรงผลักระหว่างอิเล็กตรอนตามทฤษฎี VSEPR ดังนั้น sp3 ไฮบริดออร์บิทัลจะจัดเรียงตัวเป็นทรงสี่หน้า มีมุมระหว่างไฮบริดออร์บิทัลเป็น 109.50 จากนั้นคาร์บอนจะใช้ sp3 ไฮบริดออร์บิทัลซ้อนกับ 1s ออร์บิทัลของไฮโดรเจนอะตอมเกิดพันธะระหว่างคาร์บอนและไฮโดรเจน 4 พันธะ
ภาที่ 28 การเกิด sp3 ไฮบริดออร์บิทัล 4 ออร์บิทัล ซึ่งจัดเรียงตัวเป็นทรงสี่หน้า
ภาพการเกิดพันธะ
ระหว่างคาร์บอนและไฮโดรเจนใน CH4 โดยคาร์บอนใช้ sp3ไฮบริดออร์บิทัลซ้อนกับ 1s ออร์บิทัลของไฮโดรเจน ทำให้โมเลกุลของ CH4 มีรูปร่างเป็นทรงสี่หน้าไฮบริไดเซชันของ s ออร์บิทัล 1 ออร์บิทัล และ p ออร์บิทัล 1 ออร์บิทัล ทำให้เกิด sp ไฮบริดออร์บิทัลจำนวน 2 ออร์บิทัลซึ่งมีรูปร่างเหมือนกันและมีพลังงานเท่ากัน จัดเรียงตัวเป็นเส้นตรงทำมุม 1800 ซึ่งกันและกัน ดังรูป
ภาพ sp ไฮบริไดเซชันและ sp ไฮบริดออร์บิทัล
จากทฤษฎี VSEPR ทำนายว่าโมเลกุล BeF2 เป็นเส้นตรง ถ้าใช้ทฤษฎีไฮบริดออร์บิทัลอธิบายการเกิดพันธะ รูปร่างของโมเลกุล BeF2 จะเป็นอย่างไร
ฟลูออรีนมีโครงสร้างอิเล็กตรอนเป็น 1s2 2s2 2p5
โดยมีอิเล็กตรอนเดี่ยว 1 ตัว ใน 2p ออร์บิทัล จึงสามารถเกิดพันธะ σ ได้ 1 พันธะ Be อะตอมมีโครงสร้างอิเล็กตรอนเป็น 1s2 2s2 การจัดอิเล็กตรอนในออร์บิทัลอะตอมในสภาวะพื้น Be ไม่มีอิเล็กตรอนเดี่ยว จึงไม่น่าจะเกิดพันธะโคเวเลนต์กับ F อะตอมได้ แต่อิเล็กตรอนใน 2s ออร์บิทัลของ Be อะตอมอาจถูกส่งเสริม (promotion) ให้ขึ้นไปอยู่ใน 2p ออร์บิทัลได้ ทำให้ Be มีอิเล็กตรอนเดี่ยว 2 ตัวอยู่ใน 2s และ 2p ออร์บิทัล 2s และ 2p ออร์บิทัลดังกล่าวจะรวมกันเกิด sp ไฮบริดออร์บิทัล 2 ออร์บิทัลซึ่งมีรูปร่างเหมือนกันและมีพลังงานเท่ากัน ทำมุม 180 º ซึ่งกันและกัน จากนั้น sp ไฮบริดออร์บิทัลทั้งสองจะเกิดการซ้อนกับ p ออร์บิทัลของฟลูออรีน เกิดเป็นพันธะ σ สองพันธะ
ภาพแสดงออร์บิทัลอะตอมและการเกิดไฮบริไดเซชันของ Be ใน BeF2
ภาพการเกิดพันธะโคเวเลนต์ใน BeF2
โดยการซ้อนกันของ sp ไฮบริดออร์บิทัลของ Be กับ p ออร์บิทัลของ F
ภาพ sp2 ไฮบริไดเซชันและ sp2 ไฮบริดออร์บิทัล
ในโมเลกุลที่มีรูปร่างเป็นสามเหลี่ยมแบนราบ อะตอมกลางจะมี sp2 ไฮบริดออร์บิทัล เช่น โมเลกุลของ BF3 อิเล็กตรอนจาก 2s ออร์บิทัลของ B อะตอมจะถูกกระตุ้นขึ้นไปอยู่ที่ 2p ออร์บิทัล แล้ว s ออร์บิทัล 1 ออร์บิทัล และ p ออร์บิทัล 2 ออร์บิทัล ซึ่งบรรจุอิเล็กตรอนเดี่ยว เกิดไฮบริไดเซชันเป็น sp2 ไฮบริดออร์บิทัล 3 ออร์บิทัล ทำมุม 1200 ซึ่งกันและกัน sp2 ไฮบริดออร์บิทัลเหล่านี้จะซ้อนกับ p ออร์บิทัลของ F เกิดพันธะ สามพันธะโมเลกุล BF3 จึงมีรูปร่างเป็นสามเหลี่ยมแบนราบ
แผนภาพแสดงออร์บิทัลอะตอมและการเกิดไฮบริไดเซชั่นของ B ใน BF3
ภาพที่ 35 การเกิดพันธะโคเวเลนต์ในโมเลกุล BF3
โดย sp2 ไฮบริดออร์บิทัลของ B ซ้อนกับ 2p ออร์บิทัลของ F
พิจารณาการเกิดพันธะใน CH4 คาร์บอนอะตอมกลางในสภาวะพื้นจะถูกกระตุ้นให้เวเลนซ์อิเล็กตรอนจาก 2s ออร์บิทัลขึ้นไปอยู่ใน 2p ออร์บิทัลซึ่งมีพลังงานสูงขึ้น จากนั้น 2s ออร์บิทัล 1 ออร์บิทัล และ 2p ออร์บิทัล 3 ออร์บิทัลจะรวมกันเกิดเป็น sp3 ไฮบริดออร์บิทัล จำนวน 4 ออร์บิทัล
แผนภาพแสดงออร์บิทัลอะตอมและการเกิดไฮบริไดเซชันของ C ใน CH4
sp3 ไฮบริดออร์บิทัลของคาร์บอนอะตอมสามารถซ้อนกับ 1s ออร์บิทัลของไฮโดรเจนอะตอม เกิดเป็นพันธะโคเวเลนต์ โดยรูปร่างของโมเลกุล CH4 เป็นทรงสี่หน้า ในโมเลกุลของ BeF2, BF3 และ CH4 อะตอมของ Be, B และ C สามารถใช้ไฮบริดออร์บิทัลที่บรรจุอิเล็กตรอนเดี่ยว ซ้อนกับออร์บิทัลของอะตอมอื่นเกิดเป็นพันธะ อย่างไรก็ตาม ไฮบริดออร์บิทัลอาจมีอิเล็กตรอนบรรจุอยู่ 2 ตัวก็ได้ ในกรณีเช่นนี้อะตอมจะไม่สามารถใช้ไฮบริดออร์บิทัลนั้นสร้างพันธะกับอะตอมอื่น เนื่องจากตามหลักการกีดกันของพาวลี แต่ละออร์บิทัลบรรจุอิเล็กตรอนได้เพียง 2 ตัวเท่านั้น เราจึงเรียกอิเล็กตรอนในไฮบริดออร์บิทัลดังกล่าวว่า “อิเล็กตรอนคู่โดดเดี่ยว” ตัวอย่างเช่น โมเลกุลของ NH3 และ H2O ซึ่งมีรูปทรงเรขาคณิตของคู่อิเล็กตรอนรอบอะตอมกลางเป็นทรงสี่หน้าดังนั้นออร์บิทัลอะตอมจึงเกิดไฮบริไดเซชันให้ sp3 ไฮบริดออร์บิทัล 4 ออร์บิทัล NH3 โมเลกุล sp3 ไฮบริดออร์บิทัลของไนโตรเจนอะตอม 3 ออร์บิทัลบรรจุอิเล็กตรอนเดี่ยว จึงสามารถเกิดพันธะ σ สามพันธะกับไฮโดรเจน 3 อะตอม ส่วนอีกหนึ่งออร์บิทัลบรรจุคู่อิเล็กตรอนที่ไม่สร้างพันธะหรืออิเล็กตรอนคู่โดดเดี่ยว
ภาพไฮบริดไดเซชันของไนโตรเจนในโมเลกุลของแอมโมเนีย ( NH3 )
ทฤษฎี VSEPR ทำนายได้ว่ารูปทรงเรขาคณิตของคู่อิเล็กตรอนเป็นทรงสี่หน้า โดยมีอิเล็กตรอนคู่โดดเดี่ยวหนึ่งคู่ ระบุชนิดของไฮบริดออร์บิทัลที่มีการจัดเรียงตัวสอดคล้องกับรูปทรงเรขาคณิตของคู่อิเล็กตรอน การที่คู่อิเล็กตรอนจัดเรียงตัวเป็นทรงสี่หน้า แสดงให้เห็นว่ามีออร์บิทัลที่มีรูปร่างและพลังงานเหมือนกัน 4 ออร์บิทัล นั่นคือ N อะตอมเกิด ไฮบริดออร์บิทัลใน H2O โมเลกุล sp3 ไฮบริดออร์บิทัลของออกซิเจนอะตอม 2 ออร์บิทัลบรรจุอิเล็กตรอนเดี่ยว จึงเกิดพันธะ สองพันธะกับไฮโดรเจน 2 อะตอม ส่วนอีก 2 ออร์บิทัลบรรจุอิเล็กตรอนคู่โดดเดี่ยว
ภาพไฮบริไดเซชันของออกซิเจนในโมเลกุลของน้ำ (H2O)
อะตอมในคาบที่ 3 ขึ้นไป สามารถใช้ d ออร์บิทัลในการเกิดไฮบริดออร์บิทัลได้ ไฮบริดออร์บิทัลที่เกี่ยวข้องกับ d ออร์บิทัลที่สำคัญที่สุดคือ sp3d และ sp3d2ไฮบริดออร์บิทัล จะเห็นว่า sp3dไฮบริดออร์บิทัล ชี้ไปยังมุมของพีระมิดคู่ฐานสามเหลี่ยม และ sp3d2 ไฮบริดออร์บิทัลชี้ไปยังมุมของทรงแปดหน้า
ภาพรูปร่างของ sp3 d และ sp3 d2 ไฮบริดออร์บิทัล
ตารางที่ 3 แสดงลักษณะเฉพาะในการจัดเรียงตัวเป็นรูปทรงเรขาคณิตของไฮบริดออร์บิทัล
ไฮบริไดเซชันในโมเลกุลที่มีพันธะคู่และพันธะสาม
สำหรับโมเลกุลที่อะตอมกลางเกิดพันธะคู่และพันธะสาม ไฮบริดออร์บิทัลจะบรรจุอิเล็กตรอนคู่สร้างพันธะ σ ในพันธะเดี่ยว π พันธะคู่หรือพันธะสาม และอิเล็กตรอนคู่โดดเดี่ยวเท่านั้น ส่วนอิเล็กตรอนที่ใช้ในการสร้างพันธะในพันธะคู่หรือพันธะสามนั้นจะบรรจุในออร์บิทัลอะตอมที่ไม่ได้เกิดไฮบริไดเซชัน
พิจารณาการเกิดพันธะในเอทีน (ethene) หรือเอทิลีน (ethylene) ซึ่งมีสูตรเป็น C2H4 และโครงสร้างลิวอิสเป็นดังนี้
รอบคาร์บอนแต่ละอะตอม โมเลกุลจะมีรูปร่างเป็นสามเหลี่ยมแบนราบโดยมีมุมพันธะเป็น sp2 ดังนั้นทุกอะตอมในโมเลกุลจึงอยู่ในระนาบเดียวกัน จากโครงสร้างโมเลกุลแสดงว่าแต่ละคาร์บอนอะตอมใช้ sp2 ไฮบริดออร์บิทัลในการเกิดพันธะสอง σ พันธะกับไฮโดรเจน 2 อะตอม และเกิดพันธะ σ หนึ่งพันธะกับคาร์บอนอีกอะตอมหนึ่ง
จากแผนภาพแสดงออร์บิทัลอะตอมและการเกิด sp2 ไฮบริไดเซชัน อาจเขียนโครงสร้างอิเล็กตรอนของคาร์บอนโดยพิจารณาเวเลนซ์ออร์บิทัลได้ดังนี้
จะเห็นว่าคาร์บอนยังมีอิเล็กตรอนเดี่ยวใน 2 p ออร์บิทัล ที่ไม่เกิดไฮบริไดเซชัน p ออร์บิทัลนี้มีทิศทางตั้งฉากกับระนาบสามเหลี่ยมแบนราบของ sp2 ไฮบริดออร์บิทัล จึงสามารถซ้อนกันทางด้านข้างเกิดพันธะ π ได้
แผนภาพแสดงออร์บิทัลอะตอมและการเกิดไฮบริไดเซชันของ C ใน เอทีน หรือ เอทิลีน (C2H4 )
ภาพการซ้อนกันของ p ออร์บิทัลที่ไม่เกิดไฮบริไดเซชัน เกิดเป็นพันธะ π
จากรูปการเกิดพันธะคู่ระหว่างคาร์บอน-คาร์บอน C=C ในเอทีน หรือ เอทิลีน (C2H4) พิจารณาโมเลกุลของเอไทน์ (ethyne) หรืออะเซทิลีน (acethylene, (C2H2 ) ซึ่งเป็นแก๊สที่ใช้เป็นเชื้อเพลิงสำหรับเชื่อมโลหะ
โมเลกุลของเอไทน์เป็นเส้นตรง แต่ละคาร์บอนต้องใช้ sp ไฮบริดออร์บิทัลในการเกิดพันธะ กับคาร์บอนอีกอะตอมหนึ่ง และกับไฮโดรเจน จากโครงสร้างอิเล็กตรอนของคาร์บอนเมื่อเกิด sp ไฮบริไดเซชัน
จะเห็นว่าแต่ละคาร์บอนอะตอมจะมีอิเล็กตรอนเดี่ยวอีก 2 อิเล็กตรอนอยู่ใน p ออร์บิทัลที่ไม่ได้ไฮบริไดซ์ทั้งสองออร์บิทัล ซึ่งอยู่ในแนวตั้งฉากกับ sp ไฮบริดออร์บิทัล p ออร์บิทัลทั้งสองจึงสามารถซ้อนกัน เกิดเป็นพันธะสองพันธะ ดังนั้น พันธะสามจึงประกอบด้วยพันธะ หนึ่งพันธะ σ และพันธะ π สองพันธะ
ภาพการเกิดพันธะสามระหว่างคาร์บอน-คาร์บอน (C=C) ในเอไทน์หรืออะเซทิลีน (C2H2)
เนื่องจากพันธะ π แข็งแรงน้อยกว่าพันธะ σ ดังนั้นพันธะสาม C=C จะแข็งแรงกว่า (ความยาวพันธะน้อยกว่า) พันธะคู่ แต่แข็งแรงกว่า C – C ไม่ถึงสามเท่า ลักษณะที่สำคัญอีกประการหนึ่งของพันธะคู่และพันธะสาม คือการหมุนบิดโมเลกุลรอบแกนของพันธะคู่หรือพันธะสามไม่สามารถเกิดขึ้นได้ เช่น ใน C2H4 ถ้าเราหมุน C อะตอม รอบพันธะ (c = c) p ออร์บิทัลที่ไม่เกิดไฮบริไดเซชันบนคาร์บอนนั้นจะมีทิศทางเปลี่ยนไป ไม่อยู่ในแนวขนานกับ p ออร์บิทัลที่ไม่เกิดไฮบริดไดเซชันบนคาร์บอนอีกอะตอมหนึ่งจึงไม่สามารถซ้อนกันได้อย่างมีประสิทธิผล ดังนั้นการหมุนบิดโมเลกุลรอบพันธะคู่หรือพันธะสาม จึงทำให้เกิดการสลายพันธะ π ซึ่งต้องใช้พลังงานสูงกว่าพลังงานของโมเลกุลที่สภาวะปกติ เป็นเหตุให้การหมุนบิดรอบแกนของพันธะคู่หรือพันธะสามไม่เกิดขึ้น
ภาพการหมุนบิดโมเลกุลรอบพันธะคู่ของคาร์บอน-คาร์บอน (C = C)
พิจารณาการเกิดพันธะในฟอร์แมลดีไฮด์ ซึ่งมีพันธะเดี่ยว C-H สองพันธะ พันธะคู่ (C = O) หนึ่งพันธะ รูปทรงเรขาคณิตของคู่อิเล็กตรอนในฟอร์แมลดีไฮด์ (H2CO) เป็นสามเหลี่ยมแบนราบ แสดงว่าคาร์บอนอะตอมเกิด sp2 ไฮบริดออร์บิทัล 3 ออร์บิทัลสำหรับสร้างพันธะ σ สามพันธะ โดยที่ sp2 ไฮบริดออร์บิทัล 2 ออร์บิทัลจะเกิดพันธะ σ กับ 1s ออร์บิทัลของไฮโดรเจน 2 อะตอม ส่วน sp2 ไฮบริดออร์บิทัลอีกออร์บิทัลหนึ่งจะซ้อนกับ sp2 ไฮบริดออร์บิทัลที่บรรจุอิเล็กตรอนเดี่ยวของออกซิเจน (โครงสร้างอิเล็กตรอนของออกซิเจนคือ 2s2 2px1 2py1 2pz1 จึงเกิด sp2 ไฮบริดออร์บิทัล และมี p ออร์บิทัลที่ไม่เกิดไฮบริไดเซชันอีก 1 ออร์บิทัล) ในแนวแกนระหว่างนิวเคลียสของคาร์บอนและออกซิเจนอะตอม จึงเกิดเป็นพันธะ σ นอกจากนี้ p ออร์บิทัลที่ไม่เกิดไฮบริไดเซชันของคาร์บอนอะตอมซึ่งอยู่ในแนวตั้งฉากกับระนาบสามเหลี่ยมแบนราบ และอยู่ในแนวขนานกับ p ออร์บิทัลที่ไม่ได้เกิดไฮบริไดเซชันของออกซิเจนซึ่งมีอเล็กตรอนเดี่ยวบรรจุอยู่ จะสามารถซ้อนกันได้ทางด้านข้าง เกิดเป็นพันธะ ดังนั้นจึงเกิดพันธะคู่ระหว่างคาร์บอนและออกซิเจนซึ่งประกอบด้วยพันธะ σ และพันธะ π อย่างละ 1 พันธะ
ภาพฟอร์แมลดีไฮด์ (H2CO)
ทฤษฎีออร์บิทัลโมเลกุล (Molecular orbital theory : MO theory)
ทฤษฎีพันธะเวเลนซ์และทฤษฎีไฮบริดออร์บิทัลอธิบายว่า พันธะโคเวเลนต์ในโมเลกุลเกิดจากการซ้อนกันของออร์บิทัลอะตอมหรือไฮบริดออร์บิทัล อิเล็กตรอนในโมเลกุลจึงอยู่ในออร์บิทัลอะตอมหรือไฮบริดออร์บิทัลของแต่ละอะตอม เช่น ใน CH4 โมเลกุล พันธะเกิดจาก 1s ออร์บิทัลของ H อะตอมและ sp3 4 ออร์บิทัล ของ C อะตอม อย่างไรก็ดี ทฤษฎีพันธะเวเลนซ์ และทฤษฎีไฮบริดออร์บิทัลไม่สามารถใช้อธิบายสเปกตรัมและสมบัติแม่เหล็กของโมเลกุลได้ เช่น ออกซิเจน (O2) มีสมบัติเป็นพาราแมกเนติก (paramagnetic) ซึ่งจะถูกดึงดูดในสนามแม่เหล็กเหนื่องจากมีอิเล็กตรอนเดี่ยว แต่ออกซิเจนอะตอมมีเวเลนซ์อิเล็กตรอน 6 ตัวซึ่งเป็นเลขคู่ ตามทฤษฎีพันธะเวเลนซ์จะทำนายได้ว่าอิเล็กตรอนทั้งหมดในโมเลกุลจะอยู่เป็นคู่ ซึ่งไม่สอดคล้องกับสมบัติพาราแมกเนติก ทฤษฎีออร์บิทัลโมเลกุล มีสมมติฐานเกี่ยวกับการเกิดพันธะ ดังนี้
1.เมื่ออะตอมเข้าใกล้กัน ออร์บิทัลอะตอมของอิเล็กตรอนวงนอกสุดจะรวมกันเกิดเป็นออร์บิทัลโมเลกุล (molecular orbital : MO) ซึ่งแสดงลักษณะเฉพาะของทั้งโมเลกุล ไม่ได้เป็นของอะตอมใดอะตอมหนึ่งในโมเลกุล โดยจำนวนออร์บิทัลโมเลกุลที่เกิดขึ้นเท่ากับจำนวนออร์บิทัลอะตอมที่มารวมกัน เช่น เมื่อไฮโดรเจน 2 อะตอมรวมกันเกิดเป็น H2 โมเลกุล 1s ออร์บิทัลจาก H อะตอมทั้งสองจะรวมกันเกิดเป็นออร์บิทัลโมเลกุล 2 ออร์บิทัลที่มีระดับพลังงานไม่เท่ากัน
2.ออร์บิทัลโมเลกุลจะจัดเรียงตัวตามลำดับพลังงานที่เพิ่มขึ้น พลังงานสัมพัทธ์ ของออร์บิทัลโมเลกุลเหล่านี้ สรุปได้จากการทดลองเกี่ยวกับสเปกตรัมและสมบัติแม่เหล็กของโมเลกุล
3.เวเลนซ์อิเล็กตรอนในโมเลกุล จะบรรจุอยู่ในออร์บิทัลโมเลกุล โดยแต่ละออร์บิทัลโมเลกุลสามารถบรรจุอิเล็กตรอนได้สูดสุด 2 ตัว ตามหลักการกีดกันของพาวลี และอิเล็กตรอนจะบรรจุอยู่ในออร์บิทัลโมเลกุลที่มีพลังงานต่ำสุดจนเต็มก่อน แล้วจึงบรรจุในออร์บิทัลโมเลกุลที่มีพลังงานสูงขึ้นตามลำดับ และการบรรจุอิเล็กตรอนในออร์บิทัลโมเลกุลเป็นไปตามกฎของฮุนด์ เช่น เมื่อมีออร์บิทัลที่มีพลังงานเท่ากันว่างอยู่ อิเล็กตรอนจะบรรจุในออร์บิทัลเหล่านี้ออร์บิทัลละ 1 ตัวก่อน ทำให้เกิดออร์บิทัลที่บรรจุอิเล็กตรอนเดี่ยว เพื่อที่จะให้เข้าใจทฤษฎีออร์บิทัลโมเลกุล ให้พิจารณาโมเลกุลอะตอมคู่ของธาตุในคาบที่ 1 ในตารางธาตุ เช่น การเกิดพันธะในโมเลกุลไฮโดรเจนและฮีเลียม การรวม 1s ออร์บิทัล เมื่ออะตอมของธาตุในคาบที่ 1 ของตารางธาตุเข้าใกล้กัน 1s ออร์บิทัลจากอะตอมทั้งสองจะรวมกันเกิดเป็นออร์บิทัลโมเลกุล 2 ออร์บิทัล ออร์บิทัลโมเลกุลออร์บิทัลหนึ่งจะมีพลังงานต่ำกว่าออร์บิทัลอะตอม การบรรจุอิเล็กตรอนในออร์บิทัลนี้จะทำให้โมเลกุลเสถียรกว่าอะตอมที่แยกกันอยู่ ดังนั้นจึงเรียกออร์บิทัลโมเลกุลที่มีพลังงานต่ำกว่าออร์บิทัลอะตอมว่า ออร์บิทัลโมเลกุลที่สร้างพันธะ (bonding molecular orbital) ส่วนออร์บิทัลโมเลกุลอีกออร์บิทัลหนึ่งจะมีพลังงานสูงกว่าออร์บิทัลอะตอม การบรรจุอิเล็กตรอนในออร์บิทัลนี้จึงทำให้โมเลกุลมีพลังงานเพิ่มขึ้นและไม่เสถียร จึงเรียกออร์บิทัลโมเลกุลนี้ว่า ออร์บิทัลที่ต้านการสร้างพันธะ (antibonding molecular orbital)
ภาพการสร้างออร์บิทัลโมเลกุลจาก 1s ออร์บิทัลโมเลกุลจาก 1s ออร์บิทัลอะตอมของไฮโดรเจนอะตอม
ในออร์บิทัลโมเลกุลที่สร้างพันธะมีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียสทั้งสอง จึงทำให้ระดับพลังงานต่ำกว่าออร์บิทัลอะตอม ส่วนในออร์บิทัลโมเลกุลที่ต้านการสร้างพันธะ โอกาสที่จะพบอิเล็กตรอนในบริเวณที่อยู่ระหว่างนิวเคลียสทั้งสองมีน้อย อิเล็กตรอนจะมีความหนาแน่นมากในบริเวณด้านนอกของโมเลกุล ออร์บิทัลที่ต้านการสร้างพันธะจึงมีพลังงานสูงกว่าออร์บิทัลอะตอม ความหนาแน่นของอิเล็กตรอนในออร์บิทัลโมเลกุลที่สร้างพันธะและออร์บิทัลโมเลกุลที่ต้านการสร้างพันธะจะสมมาตรรอบแกนระหว่างนิวเคลียสทั้งสอง ซึ่งหมายความว่าออร์บิทัลทั้งสองเป็นออร์บิทัลโมเลกุลชนิดซิกมา (sigma molecular orbital) ซึ่งใช้สัญลักษณ์ σ เครื่องหมาย * ใช้แสดงว่าเป็นออร์บิทัลที่ต้านการสร้างพันธะ และตัวอักษรด้านล่างขวาแสดงออร์บิทัลอะตอมที่ทำให้เกิดออร์บิทัลโมเลกุลนั้น ๆ เช่น ออร์บิทัลโมเลกุลที่สร้างพันธะซึ่งเกิดจากการรวมกันของ 1s ออร์บิทัลจะมีสัญลักษณ์เป็น σ 1s และออร์บิทัลโมเลกุลที่ต้านการสร้างพันธะจะมีสัญลักษณ์เป็น σ* 1s
ใน H2 โมเลกุลมีอิเล็กตรอน 2 ตัว อิเล็กตรอนทั้งสองจะบรรจุใน σ1s ออร์บิทัลซึ่งมีพลังงานต่ำกว่าก่อน
แผนภาพระดับพลังงานของออร์บิทัลโมเลกุล H2
เนื่องจากแต่ละ H อะตอมมีอิเล็กตรอน 1 ตัวใน 1s ออร์บิทัล ดังนั้น H2 จึงมีอิเล็กตรอน 2 ตัว อิเล็กตรอนทั้งสองจะบรรจุใน σ 1s ออร์บิทัลซึ่งมีพลังงานต่ำกว่าออร์บิทัลอะตอมในอะตอมเดี่ยว H2 โมเลกุลจึงเสถียรกว่า H สองอะตอมที่แยกกันอยู่
ฮีเลียม (He) แต่ละอะตอมมีอิเล็กตรอน 2 ตัวอยู่ใน 1s ออร์บิทัล เมื่อ He สองอะตอมเข้าใกล้กัน 1s ออร์บิทัลจะรวมกันเป็นออร์บิทัลโมเลกุล σ 1s และ σ* 1s อิเล็กตรอนใน He2 โมเลกุลจะบรรจุในออร์บิทัลที่สร้างพันธะ 2 ตัว และออร์บิทัลที่ต้านการสร้างพันธะ 2 ตัว เนื่องจาพลังงานที่ลดลงจากอิเล็กตรอนที่สร้างพันธะ
แผนภาพระดับพลังงานของออร์บิทัลโมเลกุลของ He2
การเกิดพันธะในโมเลกุลอะตอมคู่ของธาตุในคาบที่ 2 : การรวม 2s และ 2p ออร์บิทัล
ธาตุเรพรีเซนเททิฟในคาบที่ 2 ของตารางธาตุมีเวเลนซ์อิเล็กตรอนบรรจุใน 2s, 2px, 2py และ 2pzออร์บิทัลเมื่ออะตอมของธาตุในคาบที่ 2 เกิดพันธะกันเป็นโมเลกุลอะตอมคู่ ออร์บิทัลอะตอมที่บรรจุเวเลนซ์อิเล็กตรอนจะรวมกันเกิดเป็นออร์บิทัลโมเลกุลอย่างไร
การรวม 2s ออร์บิทัลจากแต่ละอะตอมจะให้ออร์บิทัลโมเลกุล 2 ออร์บิทัล คือ 
และ ซึ่งมีรูปร่างเหมือน
ซึ่งมีรูปร่างเหมือน และ
และ ตามลำดับ
ตามลำดับ

และ
 ซึ่งมีรูปร่างเหมือน
ซึ่งมีรูปร่างเหมือน และ
และ ตามลำดับ
ตามลำดับ
ในอะตอมเดี่ยวของธาตุในคาบที่ 2 จะมี p ออร์บิทัล 3 ออร์บิทัลคือ 2px , 2py และ 2pz ซึ่งมีทิศทางตั้งฉากซึ่งกันและกัน กำหนดให้แกนระหว่างนิวเคลียสของอะตอมที่เกิดพันธะกันคือแกน z เมื่อ 2pz ออร์บิทัลจากแต่ละอะตอมรวมกันตามแนวแกนระหว่างนิวเคลียส จะเกิดเป็นออร์บิทัลโมเลกุลที่สมมาตรรอบแกน z นั่นคือ เป็นออร์บิทัลโมเลกุลชนิดซิกมา 2 ออร์บิทัล ออร์บิทัลที่มีพลังงานต่ำกว่าจะมีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดซิกมาที่สร้างพันธะ  ส่วนออร์บิทัลที่มีพลังงานสูงกว่าจะมีความหนาแน่นของอิเล็กตรอนจะสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดซิกมาที่ต้านการสร้างพันธะ
ส่วนออร์บิทัลที่มีพลังงานสูงกว่าจะมีความหนาแน่นของอิเล็กตรอนจะสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดซิกมาที่ต้านการสร้างพันธะ ดังภาพ
ดังภาพ
 ส่วนออร์บิทัลที่มีพลังงานสูงกว่าจะมีความหนาแน่นของอิเล็กตรอนจะสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดซิกมาที่ต้านการสร้างพันธะ
ส่วนออร์บิทัลที่มีพลังงานสูงกว่าจะมีความหนาแน่นของอิเล็กตรอนจะสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดซิกมาที่ต้านการสร้างพันธะ ดังภาพ
ดังภาพ
ภาพ ออร์บิทัลโมเลกุลที่เกิดจากการรวมออร์บิทัลอะตอม (ก) 2pz (ข) 2px หรือ 2py
ออร์บิทัลอะตอม 2px หรือ 2py ซึ่งตั้งฉากกับ 2pz จะรวมกับออร์บิทัลอะตอม 2px หรือ 2py จากอีกอะตอมหนึ่งในลักษณะที่แตกต่างจาก 2pz ออร์บิทัล ดังรูป (ข) โดยจะเกิดการรวมกันทางด้านข้างทำให้เกิดออร์บิทัลโมเลกุล 2 ออร์บิทัล ซึ่งความหนาแน่นของอิเล็กตรอนในออร์บิทัลไม่สมมาตรรอบแกนระหว่างนิวเคลียส ซึ่งเป็นลักษณะของออร์บิทัลโมเลกุลชนิดพาย π (pi molecular orbital, ) ออร์บิทัลที่มีพลังงานสูงกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่ต้านการสร้างพันธะ
) ออร์บิทัลที่มีพลังงานสูงกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่ต้านการสร้างพันธะ  หรือ
หรือ ออร์บิทัลที่มีพลังงานต่ำกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่สร้างพันธะ
ออร์บิทัลที่มีพลังงานต่ำกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่สร้างพันธะ หรือ พลังงานสัมพัทธ์ของออร์บิทัลโมเลกุลในโมเลกุลอะตอมคู่ของธาตุเรพรีเซนเททิฟในคาบที่ 2 โปรดสังเกตว่าจาก Li2 ถึง N2 พลังงานของ
หรือ พลังงานสัมพัทธ์ของออร์บิทัลโมเลกุลในโมเลกุลอะตอมคู่ของธาตุเรพรีเซนเททิฟในคาบที่ 2 โปรดสังเกตว่าจาก Li2 ถึง N2 พลังงานของ และ
และ ออร์บิทัลจะต่ำกว่าพลังงานของ
ออร์บิทัลจะต่ำกว่าพลังงานของ ออร์บิทัลและตั้งแต่ O2 ถึง Ne2 พลังงานของ
ออร์บิทัลและตั้งแต่ O2 ถึง Ne2 พลังงานของ ออร์บิทัลจะต่ำกว่าพลังงานของ
ออร์บิทัลจะต่ำกว่าพลังงานของ และ
และ ออร์บิทัล
ออร์บิทัล
 ) ออร์บิทัลที่มีพลังงานสูงกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่ต้านการสร้างพันธะ
) ออร์บิทัลที่มีพลังงานสูงกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่ห่างจากนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่ต้านการสร้างพันธะ  หรือ
หรือ ออร์บิทัลที่มีพลังงานต่ำกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่สร้างพันธะ
ออร์บิทัลที่มีพลังงานต่ำกว่าคือออร์บิทัลที่มีความหนาแน่นของอิเล็กตรอนสูงในบริเวณที่อยู่ระหว่างนิวเคลียส เรียกว่า ออร์บิทัลโมเลกุลชนิดพายที่สร้างพันธะ หรือ พลังงานสัมพัทธ์ของออร์บิทัลโมเลกุลในโมเลกุลอะตอมคู่ของธาตุเรพรีเซนเททิฟในคาบที่ 2 โปรดสังเกตว่าจาก Li2 ถึง N2 พลังงานของ
หรือ พลังงานสัมพัทธ์ของออร์บิทัลโมเลกุลในโมเลกุลอะตอมคู่ของธาตุเรพรีเซนเททิฟในคาบที่ 2 โปรดสังเกตว่าจาก Li2 ถึง N2 พลังงานของ และ
และ ออร์บิทัลจะต่ำกว่าพลังงานของ
ออร์บิทัลจะต่ำกว่าพลังงานของ ออร์บิทัลและตั้งแต่ O2 ถึง Ne2 พลังงานของ
ออร์บิทัลและตั้งแต่ O2 ถึง Ne2 พลังงานของ ออร์บิทัลจะต่ำกว่าพลังงานของ
ออร์บิทัลจะต่ำกว่าพลังงานของ และ
และ ออร์บิทัล
ออร์บิทัล
แผนภาพระดับพลังงานของออร์บิทัลโมเลกุลในโมเลกุลอะตอมคู่ของธาตุในคาบที่ 2
(ก) Li2 ถึง N2 (ข) O2 ถึง Ne2
จากแผนภาพระดับพลังงานของออร์บิทัลโมเลกุล เราสามารถเขียนโครงสร้างอิเล็กตรอนในออร์บิทัลโมเลกุล ( MO electron configuration ) ของโมเลกุลอะตอมคู่ของธาตุเรพรีเซนเททิฟในคาบที่ 2 ได้ โดยบรรจุอิเล็กตรอนในออร์บิทัลโมเลกุลตามลำดับพลังงานจากต่ำไปสูง เช่น โครงสร้างอิเล็กตรอนของ F2 เขียนได้ดังนี้
สารประกอบโคเวเลนต์
สารประกอบโคเวเลนต์ มีสมบัติดังนี้
1.มีจุดเดือด จุดหลอมเหลวต่ำ เนื่องจากแรงยึดเหนี่ยวระหว่างโมเลกุลมีค่าน้อย
2.ไม่นำไฟฟ้าทั้งสภาพแก๊ส ของเหลว และของแข็ง
3.ไม่ละลายในตัวทำละลายมีขั้ว เช่น น้ำ แต่ละลายในตัวทำละลายไม่มีขั้ว เช่น เบนซิน
4.ปฏิกิริยาของสารประกอบโคเวเลนต์ เป็นปฏิกิริยาที่เกิดช้าเพราะต้องทำลายพันธะเดิมก่อนแล้วเกิดพันธะใหม่ การปะทะกันระหว่างโมเลกุลจะเกิดปฏิกิริยาเมื่อได้รับพลังงานเพียงพอ
มีสารโคเวเลนต์บางชนิดที่ไม่มีโมเลกุล ปกติมีสถานะเป็นของแข็ง ภายในโครงสร้างประกอบด้วยอะตอมชนิดเดียวกันต่อกันด้วยพันธะโคเวเลนต์เป็นโครงสร้างสามมิติขนาดใหญ่ ได้แก่ เพชร (C) ซิลิคอน (Si) ซิลิคอน
คาร์ไบด์ (SiC) เป็นต้น ซึ่งเพชรประกอบด้วยอะตอมคาร์บอนต่อกันด้วยพันธะโคเวเลนต์มีโครงสร้างแบบทรงสี่หน้าต่อกันไปเป็นโครงสร้างที่ยึดกันแน่นเป็นของแข็งที่แข็งมาก มีจุดเดือด จุดหลอมเหลวสูงถึง 3,500 องศาเซลเซียส ไม่นำไฟฟ้า นอกจากนี้ยังพบว่า คาร์บอนมีโมเลกุลที่เสถียรมากอีกแบบหนึ่งคือ มีโครงสร้างประกอบด้วยคาร์บอน 60 อะตอม แต่ละอะตอมสร้างพันธะโคเวเลนต์ด้วย sp2 ไฮบริดออร์บิทัล นักเคมีเรียกโครงสร้างแบบนี้ว่าบัคมินสเตอร์ฟุลเลอรีน (Buckminsterfullerene) นิยมเรียกสั้น ๆ ว่า บัคกีบอล (Buckyball)
พันธะโลหะ (Metallic bond)
โลหะเป็นธาตุที่มีอิเล็กตรอนระดับนอกจำนวนน้อย และมีพลังงานการแตกตัวเป็นไอออนต่ำ มีจุดหลอมเหลวสูง นำไฟฟ้าและความร้อนได้ดี สามารถทุบให้เป็นแผ่นบางหรือดึงให้เป็นเส้นได้ โลหะมีเงาและทึบแสง สมบัติเหล่านี้แสดงว่าอะตอมโลหะไม่ได้ยึดเหนี่ยวกันด้วยพันธะไอออนิก หรือพันธะโคเวเลนต์ หรือแรงแวนเดอร์วาล เหตุผลเพราะว่าสารที่มีพันธะโคเวเลนต์ ไม่นำไฟฟ้า เนื่องจากไม่มีอิเล็กตรอนที่สามารถเคลื่อนที่ไปได้ และจะทำให้เป็นแผ่นหรือดึงให้เป็นเส้นก็ไม่ได้ เพราะพันธะโคเวเลนต์มีทิศทางเฉพาะย่อมขัดขืนต่อการเปลี่ยนรูป พันธะไอออนิกก็เช่นกัน แม้เป็นพันธะที่ไม่มีทิศทาง ถ้าใช้แรงทุบตีให้เป็นแผ่นก็จะแตกหักออกจากกัน ส่วนแรงแวนเดอร์วาลเป็นแรงที่อ่อนมากแต่โลหะเป็นวัสดุที่แข็งแรงย่อมมีแรงระหว่างอนุภาคสูงมากกว่าแรงแวนเดอร์วาล
จากสมบัติของโลหะดังกล่าวแสดงว่าโลหะมีพันธะที่เป็นแรงดึงดูดระหว่างไอออนบวกที่อยู่เรียงชิดติดกันกับอิเล็กตรอนที่อยู่โดยรอบ คล้ายทะเลอิเล็กตรอนที่เคลื่อนไหลอยู่รอบ ๆ ไอออนบวกจึงเป็นเหตุทำให้โลหะนำไฟฟ้าได้ดี ตีให้เป็นแผ่นหรือดึงให้เป็นเส้นได้ โดยไม่แตกหักดังภาพ
แรงยึดเหนี่ยวระหว่างโมเลกุล (Intermolecular Forces)
แรงยึดเหนี่ยวภายในโมเลกุล นอกจากอยู่ในรูปของพันธะไอออนิกและพันธะโคเวเลนต์แล้วยังมีแรงยึดเหนี่ยวที่สำคัญระหว่างอะตอมและระหว่างโมเลกุล คือ แรงแวนเดอร์วาล (van der waal forces) และพันธะไฮโดรเจน (hydrogen bond) แรงดึงดูดทั้งสองนี้เป็นแรงที่อ่อนกว่าแรงจากพันธะไอออนิกและโคเวเลนต์ แรงดึงดูดระหว่างโมเลกุลนี้มีความสำคัญและสามารถใช้อธิบายสมบัติทางเคมีของสารและสมบัติทางกายภาพ เช่น จุดเดือด จุดหลอมเหลว แรงแวนเดอร์วาลจะเพิ่มมากขึ้นเมื่อจำนวนอิเล็กตรอนและมวลโมเลกุลเพิ่ม แรงยึดเหนี่ยวระหว่างโมเลกุลมีหลายประเภทดังนี้
แรงแวนเดอร์วาล (van der waal forces)
เป็นแรงดึงดูดระหว่างโมเลกุลไม่มีขั้วซึ่งเป็นผลมาจากการมีสภาพขั้วขณะหนึ่ง ซึ่งภายในอะตอมหรือโมเลกุลมีกลุ่มอิเล็กตรอนเคลื่อนที่ตลอดเวลา ความหนาแน่นของอิเล็กตรอนรอบ ๆ นิวเคลียสเปลี่ยนแปลงได้ทำให้ชั่วขณะหนึ่ง มีความหนาแน่นของอิเล็กตรอนไม่สม่ำเสมอ เป็นผลทำให้เกิดลักษณะขั้วบวกลบ (สองขั้ว) ขึ้นมาชั่วขณะ นั่นคือ ศูนย์กลางของประจุบวกเคลื่อนที่ไปอยู่คนละที่กับศูนย์กลางของประจุลบ โมเลกุลเหล่านี้จะเหนี่ยวนำโมเลกุลที่อยู่ข้างเคียงให้กลายเป็นโมเลกุลที่มีขั้วขึ้นมาด้วย และมีแรงดึงดูดกันแม้เป็นช่วงระยะเวลาสั้น ๆ แต่เกิดบ่อยครั้ง แรงดึงดูดจึงมีอยู่ตลอดไป นอกจากนี้ขนาดและรูปร่างโมเลกุลก็มีส่วนสำคัญ โมเลกุลขนาดใหญ่และมีรูปร่างยาวจะอยู่ในสภาพมีขั้วง่ายกว่าโมเลกุลที่มีขนาดเล็กและมีรูปร่างเป็นก้อนกลม
แรงดึงดูดระหว่างขั้ว (dipole-dipole interaction)
แรงนี้เกิดจากโมเลกุลที่มีขั้ว เช่น CO, NO, SO2 เมื่อโมเลกุลเหล่านี้เข้ามาใกล้กัน ขั้วบวก (137) ของโมเลกุลจะหันเข้าหาด้านขั้วลบ (138) ของอีกโมเลกุลหนึ่ง ทำให้เกิดแรงดึงดูดขึ้น ซึ่งเป็นแรงดึงดูดที่อ่อน มีความแรงประมาณ 1% ของพันธะไอออนิกหรือพันธะโคเวเลนต์เท่านั้น แรงดึงดูดประเภทนี้ทำให้โมเลกุลที่มีสภาพขั้ว มีจุดเดือดจุดหลอมเหลวสูงกว่าโมเลกุลที่ไม่มีสภาพขั้ว เมื่อมีมวลโมเลกุลใกล้เคียงกัน
พันธะไฮโดรเจน (Hydrogen bond)
พันธะไฮโดรเจน เป็นพันธะที่เกิดกับโมเลกุลที่ประกอบด้วยธาตุไฮโดรเจน (H) สร้างพันธะโคเวเลนต์กับอะตอมที่มีสภาพไฟฟ้าลบสูง ซึ่งสามารถดึงดูดอิเล็กตรอนคู่ในพันธะได้ดี ความหนาแน่นอิเล็กตรอนจะไปเข้มข้นอยู่ทางด้านของอะตอมที่มีสภาพไฟฟ้าลบสูง ทำให้อะตอมไฮโดรเจนมีสภาพไฟฟ้าเป็นบวกมาก จนเกือบกลายเป็นไฮโดรเจนไอออน อะตอมไฮโดรเจนจึงสามารถดึงดูดอะตอมที่มีสภาพไฟฟ้าลบสูงของโมเลกุลข้างเคียง เกิดเป็นพันธะขึ้น ซึ่งพันธะนี้ทำหน้าที่คล้ายสะพานเชื่อมระหว่างสองอะตอมของสองโมเลกุลนั้น พันธะไฮโดรเจนจัดเป็นแรงระหว่างโมเลกุลที่เป็นแรงดึงดูดทางไฟฟ้าอย่างอ่อนกว่าพันธะไอออนิกและพันธะโคเวเลนต์แต่แรงกว่าแรงแวนเดอร์วาล และเป็นพันธะที่ยาวกว่าพันธะโคเวเลนต์ เราใช้ขีด —- และ …. แทนพันธะไฮโดรเจน ตัวอย่าง
สารประกอบที่มีพันธะไฮโดรเจนได้แก่ HCl, H2O, HF ฟลูออรีนเป็นธาตุที่มีสภาพไฟฟ้าลบสูงที่สุด ดังนั้นพันธะ H – F ในไฮโดรเจนฟลูออไรด์จึงเป็นพันธะที่อยู่ในสภาพมีขั้วมาก จึงเกิดแรงดึงดูดระหว่างฟลูออรีนกับไฮโดรเจนของอีกโมเลกุลหนึ่ง เกิดเป็นพันธะไฮโดรเจน ดังนี้
โมเลกุลของน้ำ (H2O) เกิดพันธะไฮโดรเจนได้เป็นอย่างดี เนื่องจากออกซิเจนมีอิเล็กตรอนคู่โดดเดี่ยว 2 คู่ เช่น140 และออกซิเจนเป็นธาตุที่มีความสามารถในการดึงอิเล็กตรอนในพันธะได้ดี จึงมีความหนาแน่นของอิเล็กตรอนรอบ ๆ อะตอมออกซิเจนสูง ในขณะที่ความหนาแน่นของอิเล็กตรอนรอบอะตอมไฮโดรเจนมีเบาบางจึงเกิดพันธะไฮโดรเจนระหว่างโมเลกุลของน้ำได้ดี
ตัวอย่างของการเกิดพันธะไฮโดรเจน
พันธะไฮโดรเจนมีอิทธิพลต่อสมบัติของสาร เช่น ทำให้สารมีจุดหลอมเหลวและจุดเดือดสูงกว่าที่ควรจะเป็น เช่น H2S มีมวลโมเลกุล 34 มีสถานะเป็นแก๊สที่อุณหภูมิห้อง มีจุดเดือด – 60 องศาเซลเซียส ในขณะที่ H2O ซึ่งมีมวล 18 แต่มีสถานะเป็นของเหลวที่อุณหภูมิห้อง มีจุดเดือด 100 องศาเซลเซียส ทั้งนี้เนื่องจากอิทธิพลของพันธะไฮโดรเจนในโมเลกุลของน้ำ นอกจากนี้ พันธะไฮโดรเจนยังมีบทบาทมากในลักษณะโครงสร้างของโปรตีน DNA และ RNA ซึ่งเป็นโมเลกุลของสิ่งมีชีวิต
เลขออกซิเดชัน (Oxidation number)
เลขออกซิเดชัน หมายถึง ตัวเลขที่แสดงจำนวนอิเล็กตรอนในระดับนอกของธาตุที่ใช้ในการสร้างพันธะเคมี เวลาเขียนจะแสดงเครื่องหมายบวกหรือลบกำกับไว้ สำหรับสารประกอบไอออนิก เลขออกซิเดชันของธาตุที่ให้อิเล็กตรอนจะมีเครื่องหมายเป็นบวก และมีค่าเท่ากับจำนวนอิเล็กตรอนที่ให้ไป ส่วนธาตุที่รับอิเล็กตรอนเลขออกซิเดชันจะมีเครื่องหมายเป็นลบ และมีค่าเท่ากับจำนวนอิเล็กตรอนที่รับมา ตัวอย่างเช่น
NaCl จะได้ว่า Na มีเลขออกซิเดชันเป็น +1
Cl มีเลขออกซิเดชันเป็น -1
CaCl2 จะได้ว่า Ca มีเลขออกซิเดชันเป็น +2
Cl มีเลขออกซิเดชันเป็น -1
สำหรับสารประกอบโคเวเลนต์ที่พันธะประกอบด้วยธาตุที่มีค่าอิเล็กโทรเนกาติวิตี้สูงกับธาตุที่มีค่าอิเล็กโทรเนกาติวิตี้ต่ำ ธาตุที่มีค่าอิเล็กโทรเนกาติวิตี้สูงสามารถดึงอิเล็กตรอนคู่ที่ใช้ร่วมกันในพันธะได้ดีกว่า จะมีเลขออกซิเดชันเป็นลบ และมีค่าเท่ากับจำนวนอิเล็กตรอนที่ดึงเข้ามา ส่วนธาตุที่มีค่าอิเล็กโทรเนกาติวิตี้ต่ำกว่า จะมีเลขออกซิเดชันเป็นบวก และมีค่าเท่ากับจำนวนอิเล็กตรอนที่ถูกดึงไป
ตัวอย่างที่ 1 H2O
O มีเลขออกซิเดชัน = – 2
H มีเลขออกซิเดชัน = + 1
สำหรับธาตุหรือสารประกอบโคเวเลนต์ที่ประกอบด้วยธาตุที่มีค่าอิเล็กโทรเนกาติวิตี้เท่ากันจะมีเลขออกซิเดชันเป็นศูนย์ เช่น O2, F2, O3, S8, Cu, Fe
ข้อควรจำ ผลบวกของเลขออกซิเดชันของอะตอมทั้งหมดในสารหนึ่งโมเลกุลมีค่าเป็นศูนย์ และผลบวกของเลขออกซิเดชันของอะตอมทั้งหมดในไอออนที่มีหลายอะตอมมีค่าเท่ากับประจุของไอออนนั้น (การคิดเลขออกซิเดชันจะคิดต่อ 1 อะตอมของแต่ละธาตุ)
ตัวอย่างที่ 2 CH3Cl
C มีเลขออกซิเดชัน = – 2
Cl มีเลขออกซิเดชัน = – 1
H มีเลขออกซิเดชัน = + 1 (มี 3 อะตอม จะมีค่า = +3)
ผลรวมของเลขออกซิเดชันของ CH3Cl = 0
ตัวอย่างที่ 3 MnO4–
เนื่องจากในการสร้างพันธะเคมีของ O จะใช้ 2 อิเล็กตรอน ดังนั้น O 1 อะตอมมีเลขออกซิเดชัน – 2 ดังนั้นในไอออน MnO4– จะได้ว่า O ทั้งหมด 4 อะตอมมีเลขออกซิเดชันรวม = – 8
Mn จะมีเลขออกซิเดชัน คือ = + 7
การหาเลขออกซิเดชันของธาตุในสารประกอบพิจารณาง่าย ๆ ดังตัวอย่าง
H2SO4 H 1 อะตอมมีเลขออกซิเดชัน = +1
H 2 อะตอมมีเลขออกซิเดชัน = +2
O 1 อะตอมมีเลขออกซิเดชัน = -2
O 4 อะตอมมีเลขออกซิเดชัน = -8
ดังนั้น S 1 อะตอมจะมีเลขออกซิเดชัน = 8 – 2 = 6 แต่ผลรวมของเลขออกซิเดชันของธาตุทุกอะตอมใน 1 โมเลกุลของสารมีค่า 0 ดังนั้น S มีเลขออกซิเดชัน = + 6
สารประกอบ และสมบัติของสารประกอบ
การเกิดสารประกอบ
สารประกอบ คือ สารที่เกิดจากการรวมตัวของธาตุตั้งแต่สองธาตุขึ้นไป โดยเกิดการเคลื่อนย้ายอิเล็กตรอน เพื่อให้เป็นไปตามกฎออกเตต (ให้อิเล็กตรอนวงนอกสุดครบแปด) นั่นคือ สารประกอบเกิดจากพันธะเคมีซึ่งอาจเกิดจากพันธะไอออนิก หรือ พันธะโคเวเลนต์ก็ได้
สมบัติของสารประกอบไอออนิก
1.มีขั้ว สารประกอบไอออนิกไม่เกิดเป็นโมเลกุลเดี่ยว แต่เป็นของแข็งประกอบด้วยไอออนจำนวนมากยึดเหนี่ยวกันด้วยแรงยึดเหนี่ยวทางไฟฟ้า
2.นำไฟฟ้าได้ เมื่อใส่สารประกอบไอออนิกลงในน้ำ ไอออนจะแยกออกจากกัน ทำให้สารละลายนำไฟฟ้าได้ และสารประกอบไอออนิกที่หลอมเหลวก็นำไฟฟ้าได้ เพราะเมื่อหลอมเหลวไอออนจะแยกกันเป็นอิสระ
3.มีจุดเดือดและจุดหลอมเหลวสูง เพราะสารประกอบไอออนิกต้องใช้พลังงานมากในการทำลายแรงยึดเหนี่ยวระหว่างไอออน เพื่อจะให้กลายเป็นของเหลว หรือกลายเป็นไอ
4.การละลาย สารประกอบไอออนิกละลายได้ในน้ำหรือละลายในตัวทำละลายที่มีสภาพขั้วสูงมาก
5.การเกิดปฏิกิริยาไอออนิก เป็นปฏิกิริยาระหว่างไอออน เพราะสารประกอบไอออนิกเมื่อเป็นสารละลาย ไอออนเป็นอิสระ จึงเกิดปฏิกิริยาทันที
6.สารประกอบไอออนิกเกิดจากไอออนประจุตรงกันข้าม รอบ ๆ ไอออน จะมีสนามไฟฟ้าจึงไม่แสดงทิศทางพันธะไอออนิก
สมบัติของสารประกอบโคเวเลนต์
1.แรงดึงดูดภายในโมเลกุลมีน้อยทำให้มีสถานะเป็นแก๊ส ของเหลว และเป็นของแข็งที่อ่อนนุ่มที่อุณหภูมิปกติ
2.ไม่ละลายน้ำ
3.มีจุดเดือดและจุดหลอมเหลวต่ำ เพราะใช้พลังงานน้อยในการทำลายแรงยึดเหนี่ยวภายในโมเลกุล
4.ไม่นำไฟฟ้า
5.ละลายในเบนซีน และสารอินทรีย์หรือตัวทำละลายที่ไม่มีขั้ว
เนื่องจากสารประกอบมีอยู่มากมาย จึงจำเป็นต้องมีกฎเกณฑ์ในการเขียนสูตร และการเรียกชื่อสารประกอบ เพื่อให้สะดวกแก่การจดจำ และง่ายต่อการเรียนการสอน ทั้งจะได้มีแบบแผนหลักเกณฑ์ที่เหมือนกัน จึงมีหลักดังนี้
การเขียนสูตรสารประกอบ
สารประกอบเกิดจากการรวมตัวของธาตุ หรือหมู่ธาตุ ตั้งแต่ 2 ธาตุขึ้นไป ซึ่งอาจจะอยู่ในลักษณะของไอออน หรืออะตอมก็ได้ ในการเขียนสูตรจึงมีกฎเกณฑ์ดังนี้
1.โลหะ กับอโลหะ ให้เขียนสัญลักษณ์โลหะก่อน แล้วเขียนอโลหะตามหลัง เช่น
2.ถ้าเป็นไอออน กับไอออน ต้องเขียนไอออนบวกก่อน แล้วตามด้วยไอออนลบ เช่น
NH4 + กับ SO4 – เขียนได้เป็น ( NH4)2SO4
การเรียกชื่อสารประกอบ
การเรียกชื่อสารประกอบใช้หลักการตามระบบ IUPAC (International Union of Pure and Applied Chemistry) ซึ่งมีข้อตกลงดังนี้
1.สารประกอบระหว่างโลหะกับอโลหะ ให้เรียกชื่อโลหะธาตุแรก หรือไอออนบวก เต็ม ๆ แล้วตามด้วยอโลหะ หรือไอออนลบ แล้วเปลี่ยนท้ายเสียงเป็นไอด์ (ide) เช่น
Na (Sodium) กับ Cl (Chlorine) เขียนสูตร NaCl อ่านเป็น Sodium chloride
Ba (Barium) กับ S (Sulfur) เขียนสูตร BaS อ่านเป็น Barium sulfide
K (Potassium) กับ I (Iodine) เขียนสูตร KI อ่านเป็น Potassium iodide
บางธาตุมีการตัด / เติม พยางค์ท้ายก่อนเปลี่ยนท้ายเสียงเป็นไอด์ เช่น
H (Hydrogen) เป็น Hydride
N (Nitrogen) เป็น Nitride
O (Oxygen) เป็น Oxide
P (Phosphorus) เป็น Phosphide
2. สารประกอบระหว่างอโลหะ กับอโลหะ สารประกอบชนิดนี้แม้จะมีองค์ประกอบเหมือนกัน แต่บางทีมีสารได้มากกว่า 1 สาร เช่น SO2 กับ SO3 หรือ CO กับ CO2 การเรียกชื่อต้องบอกจำนวนอะตอมของแต่ละธาตุ เป็นภาษากรีก คือ 1 (mono), 2 (di), 3 (tri), 4 (treta), 5 (penta), 6 (hexa), 7 (hepta), 8 (octa), 9 (nona),10 (deca) ยกเว้นธาตุแรกมี 1 อะตอมไม่ต้องบอก เช่น
SO2 อ่านว่า Sulfur dioxide
SO3 อ่านว่า Sulfur trioxide
CO อ่านว่า Cabon monoxide
CO2 อ่านว่า Cabon dioxide
P2 O5 อ่านว่า Diphosphorus pentaoxide
3.สารประกอบที่มีไอออนบวก กับไอออนลบที่ไม่ใช่อะตอมเดี่ยว แต่เป็นไอออนที่ประกอบด้วยหมู่อะตอม เช่น Sulphateion SO42- มี S เป็นอะตอมกลาง ตามข้อตกลงให้ถือว่าไอออนที่มีลักษณะเช่นนี้ เป็นไอออนเชิงซ้อน เรียกชื่อแบบเดียวกับสารเชิงซ้อน แต่อนุโลมให้ใช้ชื่อสามัญ ถ้ามีธาตุอื่นมารวมตัวกับไอออนนี้ ก็เรียกธาตุนั้นนำหน้า เช่น
FeCl2 อ่านได้ว่า Iron (II) chloride
MnO2 อ่านได้ว่า Manganese (IV) oxide
สารประกอบเชิงซ้อน
สารประกอบที่ประกอบด้วยไอออนเชิงซ้อน มักจะมีโลหะสองชนิด ซึ่งในสารประกอบนั้นจะมีไอออน 2 ชนิดคือ ไอออนบวก (+) และไอออนลบ (-) และไอออนที่ประกอบด้วยธาตุตั้งแต่ 2 ธาตุขึ้นไปนี้เรียกว่า ไอออนเชิงซ้อนอาจเป็นไอออนบวกหรือไอออนลบก็ได้ พวกไอออนเชิงซ้อนจะมีธาตุแทรนซิชันเป็นอะตอมกลาง และมีไอออน อะตอม หรือโมเลกุลอื่น มาล้อมรอบ โดยเรียกสิ่งที่ล้อมรอบว่า ลิแกนด์ ส่วนมากแล้วลิแกนด์จะยึดเหนี่ยวกับธาตุแทรนซิชันด้วยพันธะโคเวเลนต์ หรือโคออร์ดิเนตโคเวเลนต์ หลักการอ่านชื่อสารประกอบเชิงซ้อนมีดังนี้
1.ถ้าไอออนเชิงซ้อนเป็นไอออนบวก ให้อ่านลิแกนด์นำหน้า แล้วตามด้วยเลขอะตอมกลาง โดยบอกเลขออกซิเดชันด้วย จากนั้นอ่านไอออนลบ
2.ถ้าไอออนเชิงซ้อนเป็นลบ อ่านลิแกนด์นำหน้า จากนั้น อ่านอะตอมกลางลงท้ายด้วย – ate โดยบ่งบอกเลขออกซิเดชันของธาตุด้วย
ลิแกนด์บางตัวที่ควรทราบ
Cl– อ่านว่า Chloro
Br– อ่านว่า Bromo
I– อ่านว่า Iodo
CO32- อ่านว่า Carbonate
H2O อ่านว่า Aqua
CN– อ่านว่า Cyano
NO2– อ่านว่า Nitro
NH3 อ่านว่า Ammine
ตัวอย่างการอ่านชื่อสารประกอบเชิงซ้อน
Na[FeF6] อ่านว่า Sodiumhexafluoroferrate (III)
[ K3Fe(CN)6 ] อ่านว่า Potassiumhexacyanoferrate (III)
[ ( Cu(H2O)4) SO4 ] อ่านว่า Tetraaquacopper (II) sulphate
[ ( Zn(NH3)4 ]2+ อ่านว่า Tetraamminezinc (II ) ion
[ ( Ni(CN)4 ]2 – อ่านว่า Tetracyanonickelate (II) ion
ที่มา https://chemistryprosite.wordpress.com/2017/03/16/%E0%B8%9A%E0%B8%97%E0%B8%97%E0%B8%B5%E0%B9%88-5-%E0%B8%88%E0%B8%A5%E0%B8%99%E0%B8%A8%E0%B8%B2%E0%B8%AA%E0%B8%95%E0%B8%A3%E0%B9%8C%E0%B9%80%E0%B8%84%E0%B8%A1%E0%B8%B5%E0%B9%81%E0%B8%A5%E0%B8%B0/




























































ไม่มีความคิดเห็น:
แสดงความคิดเห็น